
科目: 来源: 题型:解答题
| 实验步骤 | 实验现象 | 实验结论 |
| ①将等体积的两种无色液体分别加入A、B两个试管中. ②分别向A、B两试管中同时加入等质量(少量)的二氧化锰,观察现象.  | A试管中无明显现象 B试管中有气泡产生 | A试管中的无色液体是: 水; B试管中的无色液体是: 过氧化氢; |
查看答案和解析>>
科目: 来源: 题型:实验探究题
 所示装置可用来测定空气中氧气的含量.对该实验认识不正确的是C
所示装置可用来测定空气中氧气的含量.对该实验认识不正确的是C查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 降温,防止反应过于激烈 | |
| B. | 防止产生热量 | |
| C. | 使现象明显 | |
| D. | 防止生成物熔化后溅落瓶底,使瓶底炸裂 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 将气体通入澄清石灰水 | B. | 闻气体的气味 | ||
| C. | 用带火星的木条伸入集气瓶中 | D. | 用燃着的木条伸入集气瓶中 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①③⑤ | B. | ①②③⑤ | C. | ③④⑥ | D. | ①②③④⑤⑥ |
查看答案和解析>>
科目: 来源: 题型:实验探究题
| 氯酸钾的质量 | 催化剂的种类 | MnO2的质量 | 反应条件 | 收集45.0mL O2所需的时间(S) | |
| Ⅰ | 3.0g | MnO2 | 1.0g | 混合加热 | 21 |
| Ⅱ | xg | CuO | 1.0g | 混合加热 | 48 |

| 双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 温度 | 相同时间(10S)内产生O2体积(mL) | |
| Ⅰ | 50.0g | 1% | 0.1g | 20℃ | 9 |
| Ⅱ | 50.0g | 2% | 0.1g | 20℃ | 16 |
| Ⅲ | 50.0g | 4% | 0.1g | 20℃ | 31 |
| 时间/S | 4 | 8 | 12 | 16 | 20 | 24 | 28 | 32 | 36 | 40 |
| 气体体积/mL | 16.0 | 22.2 | 29.4 | 39.3 | 50.4 | 57.6 | 62.0 | 64.7 | 66.0 | 66.0 |
查看答案和解析>>
科目: 来源: 题型:解答题
| PX的 性质 | ①无色透明液体;②熔点13.2℃、沸点138.5℃;③密度0.86g/cm3;④有芳香气味;⑤可燃;⑥有挥发性,但比汽油低;⑦低毒,毒性与汽油相当;在致癌性上,按国际惯例属于第三类致癌物,即缺乏证据证明其具有致癌性;⑧遇火可爆炸,但爆炸性比汽油低(爆炸极限为1.1%~7.0%) |
| PX的 用途 | 化学工业的重要原料,用于纺织、塑料、建材、医药、农药等方面,如雪纺衣物、口罩、尼龙绳、塑料保鲜盒和保鲜袋等,涉及衣食住行的方方面面,目前我国每年“供”小于“需”,有近一半的PX是靠进口 |
查看答案和解析>>
科目: 来源: 题型:推断题
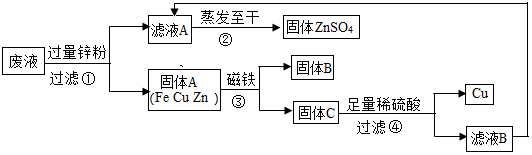 实验结束时,同学们将含有CuSO4、ZnSO4、FeSO4的废液倒在废液缸里,如果将废液直接排放就会造成水污染.于是几位同学利用课余处理废液,回收工业重要原料硫酸锌和有关金属.实验过程如图所示:
实验结束时,同学们将含有CuSO4、ZnSO4、FeSO4的废液倒在废液缸里,如果将废液直接排放就会造成水污染.于是几位同学利用课余处理废液,回收工业重要原料硫酸锌和有关金属.实验过程如图所示:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com