
科目: 来源: 题型:解答题
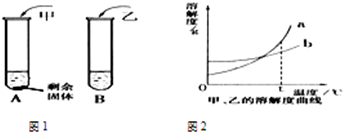
 如图是A、B两种固体物质的溶解度曲线:
如图是A、B两种固体物质的溶解度曲线:查看答案和解析>>
科目: 来源: 题型:实验探究题
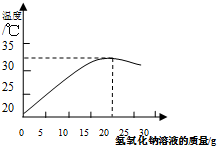 某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其测定某稀盐酸中溶质的质量分数.(已知氢氧化钠与盐酸反应会放出热量)
某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其测定某稀盐酸中溶质的质量分数.(已知氢氧化钠与盐酸反应会放出热量)查看答案和解析>>
科目: 来源: 题型:解答题
 水和溶液在生命活动和生产、生活中起着十分重要的作用.
水和溶液在生命活动和生产、生活中起着十分重要的作用.| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | NaCl | 35.7 | 36.0 | 36.5 | 37.3 | 38.4 | 39.8 |
| NH4Cl | 29.4 | 37.2 | 45.8 | 55.2 | 65.6 | 77.3 | |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:实验探究题
| 实验操作 | 实验现象 | 实验结论 |
| 取少量该溶液于试管中,向溶液中滴加足量稀盐酸,并不断振荡. | 有气泡冒出 | 该反应的方程式为 2HCl+Na2CO3═2NaCl+H2O+CO2↑,由此可知该氢氧化钠溶液一定变质了. |
| 实验步骤 | 实验现象 | 实验结论 |
| (1)取少量该溶液于试管中,向溶液中滴加过量的氯化钙溶液,并不断振荡. | 有白色沉淀 | 说明原溶液中一定有碳酸钠. 写出该反应的化学方程式CaCl2+Na2CO3=CaCO3↓+2NaCl. |
| (2)取步骤(1)试管中的少量上层清液,滴加酚酞溶液. | 溶液变红色 | 说明原溶液中一定有氢氧化钠. |
查看答案和解析>>
科目: 来源: 题型:推断题
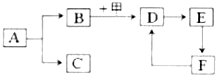 图中的物质均是初中化学常见物质,其中A、C组成元素相同,F是大理石的主要成分,甲是生活里常用的燃料.根据它们之间的转化关系(有些反应条件、反应物、生成物已省略).回答下列问题:
图中的物质均是初中化学常见物质,其中A、C组成元素相同,F是大理石的主要成分,甲是生活里常用的燃料.根据它们之间的转化关系(有些反应条件、反应物、生成物已省略).回答下列问题:查看答案和解析>>
科目: 来源: 题型:实验探究题
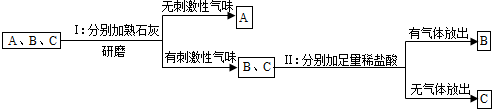
查看答案和解析>>
科目: 来源: 题型:解答题
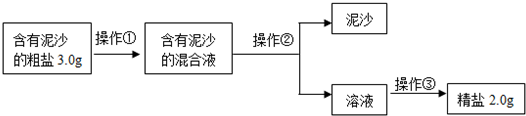
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
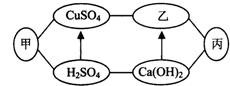 图中甲、乙、丙是初中化学中常见的物质,图中“-”表示相连的物质之间可以在溶液中发生化学反应,“→”表示由某种物质可转化为另一种物质(部分反应物、生成物及反应条件已略去).下列说法中不正确的是( )
图中甲、乙、丙是初中化学中常见的物质,图中“-”表示相连的物质之间可以在溶液中发生化学反应,“→”表示由某种物质可转化为另一种物质(部分反应物、生成物及反应条件已略去).下列说法中不正确的是( )| A. | 甲、乙、丙可能依次为Fe、NaOH、CO2 | |
| B. | 丙物质可能是氧化物也可能是酸 | |
| C. | 当乙为NaOH时,它可由Ca(OH)2与Na2CO3反应生成 | |
| D. | 上述反应共涉及到置换、化合、复分解三种基本反应类型 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com