
科目: 来源: 题型:实验探究题
 牙膏是生活必需品,某兴趣小组同学对某品牌市售牙膏展开如下探究,请回答问题:
牙膏是生活必需品,某兴趣小组同学对某品牌市售牙膏展开如下探究,请回答问题:| 实验编号 | 1 | 2 | 3 |
| 实验前(g) | 2.00 | 2.00 | 2.00 |
| 实验后(g) | 0.43 | 0.44 | 0.45 |
查看答案和解析>>
科目: 来源: 题型:实验探究题
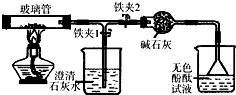
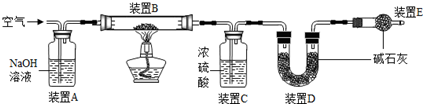
查看答案和解析>>
科目: 来源: 题型:实验探究题

| 实验内容 | 预计现象 | 预计结论 |
| 取少量废液缸中上层清液于试管中,加入过量氯化钙溶液,静置. | 小方的猜想正确. |
查看答案和解析>>
科目: 来源: 题型:实验探究题

| 实验 装置 | |
| 实验 现象 | ①无水硫酸铜粉末逐渐由白色变为蓝色 ②澄清石灰水变浑浊 |
| 结论 | 久置的镁粉中除镁元素外,还含有的元素是C、H、O 久置的镁粉中含有碱式碳酸镁 |
查看答案和解析>>
科目: 来源: 题型:实验探究题
 红枣中含有丰富的VC和糖类,常食能增强人体的免疫力,有补血养气安神等良好功效,红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图所示.某化学兴趣小组对一包久置的“504双吸剂”固体样品产生浓厚的兴趣,设计实验进行探究.
红枣中含有丰富的VC和糖类,常食能增强人体的免疫力,有补血养气安神等良好功效,红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图所示.某化学兴趣小组对一包久置的“504双吸剂”固体样品产生浓厚的兴趣,设计实验进行探究.| 实验操作 | 实验现象 | 实验结论 |
| 取少量固体于试管中,滴加足量的稀盐酸 | 固体逐渐消失,有大量无色气体产生,得到浅绿色溶液. | 固体中一定含有Fe, 一定不含Fe2O3. |

| 实验操作 | 实验现象 | 实验结论 |
| 取少量固体于试管中,滴加足量的稀盐酸,并将气体通入澄清石灰水 | 固体逐渐消失有气泡产生、澄清石灰水变浑浊,澄清石灰水变浑浊 溶液呈黄色. | 固体中一定含有CaCO3和Fe2O3. |
查看答案和解析>>
科目: 来源: 题型:实验探究题
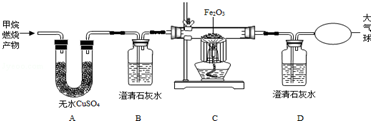
查看答案和解析>>
科目: 来源: 题型:实验探究题
 “双吸剂”是一种常见袋装食品的保鲜剂,能吸收空气中的氧气、二氧化碳、水蒸气等.化学兴趣小组的同学在某食品袋中发现一包“双吸剂”,其标签如图所示.同学们对这包久置的“双吸剂”固体样品很好奇,设计实验进行探究.
“双吸剂”是一种常见袋装食品的保鲜剂,能吸收空气中的氧气、二氧化碳、水蒸气等.化学兴趣小组的同学在某食品袋中发现一包“双吸剂”,其标签如图所示.同学们对这包久置的“双吸剂”固体样品很好奇,设计实验进行探究.| 实验操作 | 实验现象 | 实验结论 |
| ①取少量样品放入试管中,滴加一定量的 稀盐酸,用带导管的单孔橡皮塞塞紧试管口,导管另一端伸入澄清石灰水中 | 试管中固体逐渐溶解,有大量气泡产生,得到浅绿色溶液,澄清石灰水变浑浊. | 样品中一定含有 Fe、CaCO3, 不含Fe2O3. |
| ②取少量样品放入试管中,加水,静置向上层清液中滴加无色酚酞试液 | 放出大量的热量,试管底部有不溶物,酚酞试液由无色变为红色. | 样品中含有 氧化钙或氢氧化钙或二者都有. |
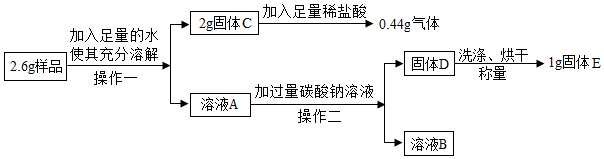
查看答案和解析>>
科目: 来源: 题型:填空题
| 可燃气体 | 爆炸极限(体积分数) |
| H2 | 4.0%~74.2% |
| CH4 | 5%~15% |
| CO | 12.5%~74.2% |

查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:实验探究题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com