
科目: 来源: 题型:实验探究题
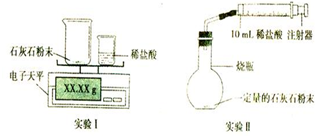
| 时间/min | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 注射器读数/ml | 60.0 | 85.0 | 88.0 | 89.0 | 89.5 | 89.8 | 89.9 | 90.0 | 90.0 | 90.0 |
查看答案和解析>>
科目: 来源: 题型:实验探究题
| 熔点 | 沸点 | 热稳定性 | 其他 |
| 101℃~102℃ | 150℃~160℃升华 | 100.1℃分解出水,175℃分解成CO2、CO、H2O | 与 Ca(OH)2反应产生白色沉淀(CaC2O4) |

查看答案和解析>>
科目: 来源: 题型:实验探究题
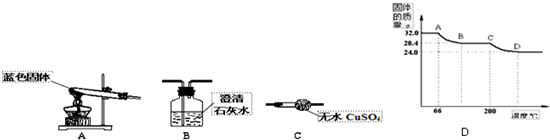
查看答案和解析>>
科目: 来源: 题型:实验探究题
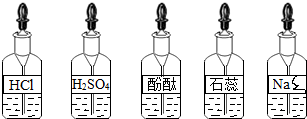
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取少量样品于试管中 向其中滴入适量的稀盐酸 | 有气泡产生 | 猜想②正确 相关的化学方程式Na2CO3+2HCl═2NaCl+H2O+CO2↑ |
查看答案和解析>>
科目: 来源: 题型:实验探究题
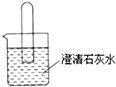 如图所示,将一个充满二氧化碳的试管倒立在盛有澄清石灰水的烧杯中,
如图所示,将一个充满二氧化碳的试管倒立在盛有澄清石灰水的烧杯中,查看答案和解析>>
科目: 来源: 题型:解答题
| 体重 | 小于等于15千克 | 15~23千克 | 23~40千克 | 大于40千克 |
| 每次用量 | 30mg | 45mg | 60mg | 60mg |
查看答案和解析>>
科目: 来源: 题型:解答题
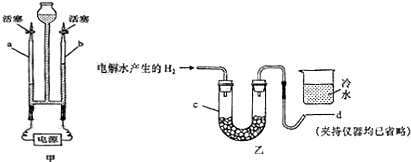
查看答案和解析>>
科目: 来源: 题型:解答题
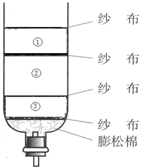 2012年3月22是第二十届“世界水日”.水与人类的生活和生产密切相关.
2012年3月22是第二十届“世界水日”.水与人类的生活和生产密切相关.查看答案和解析>>
科目: 来源: 题型:解答题
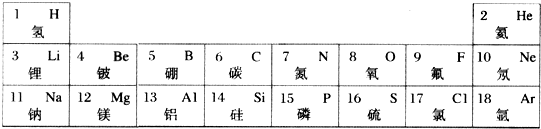
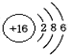 ,在化学反应中易得到电子(选填“得到”或“失去”),形成S2-(填 粒子符号).
,在化学反应中易得到电子(选填“得到”或“失去”),形成S2-(填 粒子符号).查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 空气中含有很多物质,其中只有氧气是有用的,其他成分都是有害的 | |
| B. | 空气主要供给人类呼吸,在工业农业生产上用途不大 | |
| C. | 把空气中的其他成分都分离出去,只留氧气,更有益于人类的发展 | |
| D. | 空气是多种物质组成的,是维持自然生命的支柱,防止空气污染是极其重要的 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com