
科目: 来源: 题型:实验探究题
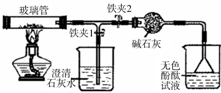
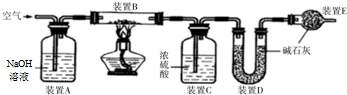
查看答案和解析>>
科目: 来源: 题型:实验探究题
| 实验方案 | 方案一:加锌粒 | 方案二:滴加酚酞溶液 |
| 实验操作 | 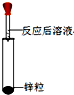 | 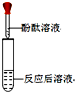 |
| 实验现象 | ⑤产生气泡 | 无明显现象 |
| 实验结论 | 溶液中有HCl | 溶液中无⑥Ca(OH)2 |
查看答案和解析>>
科目: 来源: 题型:实验探究题
| 实验步骤 | 实验现象 | 实验结论及化学方程式表示 |
| 取少量白色固体于试管中,向试管中滴加适量稀盐酸 | 有气泡 | 反应后生成的白色固体是Na2CO3 钠在二氧化碳中燃烧的化学方程式为: 4Na+3CO2$\frac{\underline{\;点燃\;}}{\;}$2Na2CO3+C |
查看答案和解析>>
科目: 来源: 题型:实验探究题
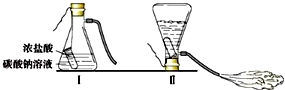
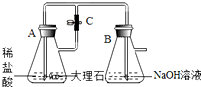 某化学实验小组的同学利用如图所示装置进行实验.A中反应开始时,弹簧夹C处于打开状态.一段时间后,关闭C,装置A中仍在反应.过一会儿,观察到装置A中液体通过长导管进入装置B,装置B中出现白色沉淀,装置A中液体能进入装置B的原因:关闭止水夹C后,A中产生的二氧化碳气体使A气压增大,大于大气压,将A中液体通过长导管压入B中,装置B中出现白色沉淀的化学反应方程式为Na2CO3+CaCl2═2NaCl+CaCO3↓.小组同学探究反应后装置B中的溶液的溶质成分.
某化学实验小组的同学利用如图所示装置进行实验.A中反应开始时,弹簧夹C处于打开状态.一段时间后,关闭C,装置A中仍在反应.过一会儿,观察到装置A中液体通过长导管进入装置B,装置B中出现白色沉淀,装置A中液体能进入装置B的原因:关闭止水夹C后,A中产生的二氧化碳气体使A气压增大,大于大气压,将A中液体通过长导管压入B中,装置B中出现白色沉淀的化学反应方程式为Na2CO3+CaCl2═2NaCl+CaCO3↓.小组同学探究反应后装置B中的溶液的溶质成分.| 实验操作 | 先向滤液中加入过量Ba(NO3)2溶液 | 然后再向滤液中滴加酚酞溶液 |
| 实验现象 | 出现白色沉淀 | 溶液变红 |
| 实验结论 | 猜想4正确 | |
查看答案和解析>>
科目: 来源: 题型:实验探究题
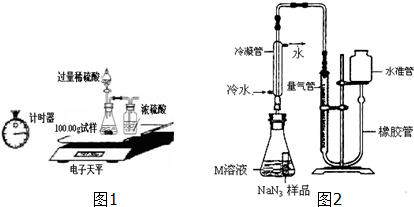
| 称量项目 | 称量时间 | 质量(g) |
| 试样 | 100.00 | |
| 装置+稀硫酸质量 | 241.20 | |
| 装置+稀硫酸质量+试样 | 反应开始后15秒 | 339.20 |
| 装置+稀硫酸质量+试样 | 反应开始后35秒 | 339.00 |
| 装置+稀硫酸质量+试样 | 反应开始后55秒 | 339.00 |
查看答案和解析>>
科目: 来源: 题型:实验探究题
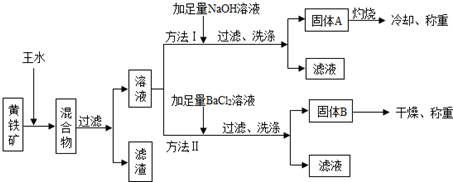
查看答案和解析>>
科目: 来源: 题型:实验探究题
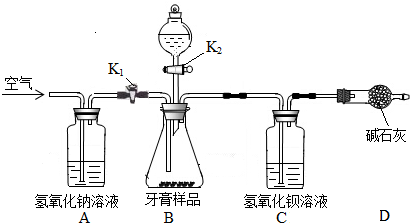
查看答案和解析>>
科目: 来源: 题型:实验探究题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
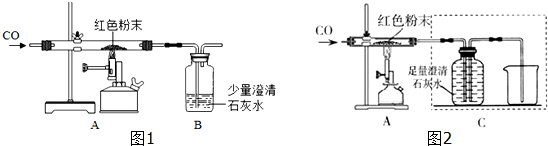
| 反应前 | 反应后 |
| 玻璃管和红色粉末的总质量为37.3g | 玻璃管和固体物质的总质量为36.1g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com