
科目: 来源: 题型:实验探究题
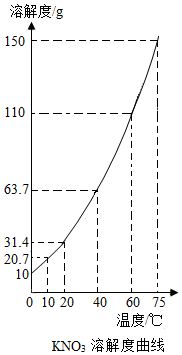 某固态混合物中含有mgKNO3和若干不溶于水的杂质,将它加入ng水中,在10℃、40℃、75℃时观察,充分溶解后的结果如表:
某固态混合物中含有mgKNO3和若干不溶于水的杂质,将它加入ng水中,在10℃、40℃、75℃时观察,充分溶解后的结果如表:| 温度 | 10℃ | 40℃ | 75℃ |
| 未溶固体 | 261g | 175g | 82g |
查看答案和解析>>
科目: 来源: 题型:实验探究题
| 测定物质 | ① | ② | ③ | ④ |
| 滴入碘水的数量(滴) | 1 | 8 | 15 | 5 |
查看答案和解析>>
科目: 来源: 题型:实验探究题
查看答案和解析>>
科目: 来源: 题型:实验探究题
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
| 实验操作 |  |  | 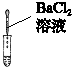 |
| 实验现象 | 试纸变色,对比比色卡,pH<7 | 有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
查看答案和解析>>
科目: 来源: 题型:实验探究题
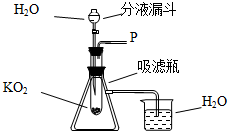 在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.首先他将少量超氧化钾(KO2)粉末用脱脂棉包裹,没有任何变化(已知脱脂棉与超氧化钾不反应),然后向包有超氧化钾(KO2)粉末的脱脂棉上滴加少量的水,则脱脂棉迅速发生剧烈的燃烧(比在空气中燃烧还剧烈).小冬对此很感兴趣,于是,他和同学们进行探究.请你也参与他们的本次探究活动.
在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.首先他将少量超氧化钾(KO2)粉末用脱脂棉包裹,没有任何变化(已知脱脂棉与超氧化钾不反应),然后向包有超氧化钾(KO2)粉末的脱脂棉上滴加少量的水,则脱脂棉迅速发生剧烈的燃烧(比在空气中燃烧还剧烈).小冬对此很感兴趣,于是,他和同学们进行探究.请你也参与他们的本次探究活动.查看答案和解析>>
科目: 来源: 题型:实验探究题
查看答案和解析>>
科目: 来源: 题型:实验探究题

查看答案和解析>>
科目: 来源: 题型:实验探究题
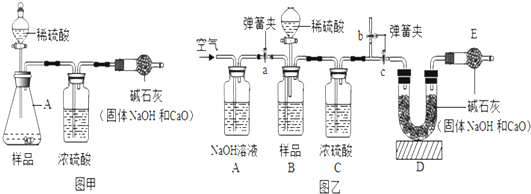
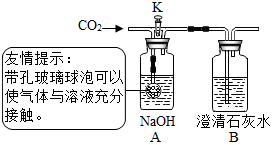 某探究小组的同学用如图所示实验装置进行实验,验证二氧化碳与氢氧化钠、氢氧化钙都能发生反应.
某探究小组的同学用如图所示实验装置进行实验,验证二氧化碳与氢氧化钠、氢氧化钙都能发生反应.| 实验步骤 | 实验现象 | 实验结论 |
| ①取滤液少许于管中,滴加Na2CO3溶液 | 无明显现象 | 猜想 三不成立 |
| ②重新取滤液少许于管中,滴入过量 氯化钙溶液,在滴入2~3滴无色酚酞 | 有白色沉淀生成,溶液变红色 | 猜想二成立 |
查看答案和解析>>
科目: 来源: 题型:实验探究题
| 实验操作步骤 | 实验目的、现象及结论 |
| (1)取少量白色固体粉末,配成水溶液,向其中加入足量的稀酸A,A为H2SO4. | 除去Na2CO3 |
| (2)继续加入足量的B,B为Ba(NO3)2溶液,过滤. | 除去H2SO4 |
| (3)向(2)中的滤液中加入C,C为 AgNO3溶液 | 若有白色沉淀生成,证明原白色固体粉末中肯定含有氯化钠;否则不含氯化钠. |
查看答案和解析>>
科目: 来源: 题型:实验探究题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com