
科目: 来源: 题型:填空题
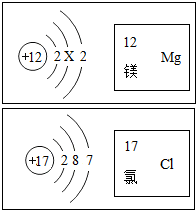 如图是镁和氯两种元素的有关信息,请回答下列问题:
如图是镁和氯两种元素的有关信息,请回答下列问题:查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:实验探究题
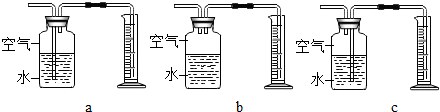
| 实验混合溶液 | 1 | 2 | 3 | 4 | 5 | 6 |
| 饱和硫酸铜溶液/mL | 0 | 0.5 | 2.5 | 5 | 10 | 20 |
| 水/mL | 20 | 19.5 | 17.5 | V | 10 | 0 |
| 实验1 | 实验2 | 实验3 | 实验4 | 实验5 | |
| 加入试剂0.5mL | 水 | 5%NaCl溶液 | 5%Mg(NO3)2溶液 | 5%FeSO4溶液 | 5%CuSO4溶液 |
| 产生气泡速率 | + | + | + | ++ | +++ |
查看答案和解析>>
科目: 来源: 题型:实验探究题
| 实验步骤 | 实验现象 | 实验结论 |
| ①取一份滤渣滴加足量稀盐酸 | 产生气泡 | 猜想三正确 |
| ②取一份滤渣加入热的蒸馏水振荡,在上层清液中再滴加无色酚酞试液 | 酚酞试液变红 |
查看答案和解析>>
科目: 来源: 题型:填空题
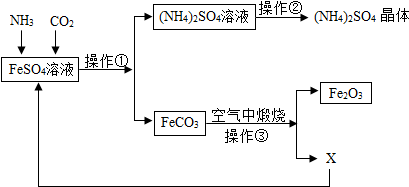
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
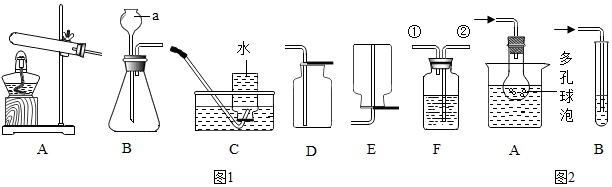
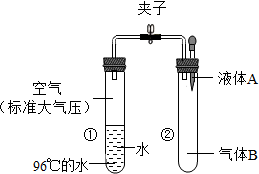 如图所示,夹子开始处于关闭状态,将液体A滴入试管②与气体B充分发生化学反应;打开夹子,可发现试管①内的水立刻沸腾了.则液体A和气体B的组合最不可能是( )
如图所示,夹子开始处于关闭状态,将液体A滴入试管②与气体B充分发生化学反应;打开夹子,可发现试管①内的水立刻沸腾了.则液体A和气体B的组合最不可能是( )| A. | 稀硫酸、二氧化碳 | B. | 盐酸、氨气 | ||
| C. | 石灰水、氯化氢 | D. | 氢氧化钠溶液、二氧化硫 |
查看答案和解析>>
科目: 来源: 题型:填空题
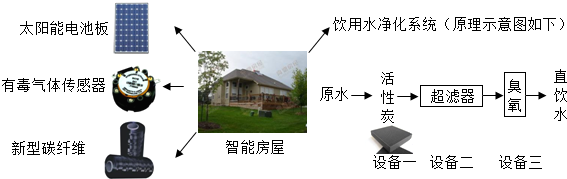
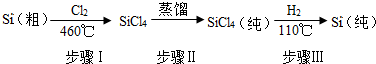
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 可能存在Cl- | B. | 一定存在CO32-,一定不存在Ba2+ | ||
| C. | 一定存在Na+ | D. | 一定存在SO42-,可能存在Ca2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com