
科目: 来源: 题型:选择题
| A. | 用酚酞鉴别食盐水和稀醋酸 | |
| B. | 用二氧化碳气体鉴别澄清石灰水和火碱溶液 | |
| C. | 用食醋鉴别厨房中的食盐和小苏打 | |
| D. | 用肥皂水鉴别硬水和软水 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 熟石灰:改良酸性土壤,制取波尔多液 | |
| B. | 干冰:人工降雨,制冷剂 | |
| C. | 一氧化碳:气体肥料冶炼金属 | |
| D. | 稀有气体和氮气:保护气 |
查看答案和解析>>
科目: 来源: 题型:计算题
| 执行标准:GB1413-99 主要成分:碳酸钙 含钙量:每片含钙0.75g 每瓶50片,重 40g (中外合资xx公司出品) |
| 物质的质量 | 第一次 | 第二次 | 第三次 | 平均值 |
| 反应前:烧杯+盐酸 | 22g | 22g | 22g | 22g |
| 10片钙片 | 8g | 8g | 8g | 8g |
| 反应后:烧杯十剩余物 | 26.7g | 26.5g | 26.9g | 26.7g |
查看答案和解析>>
科目: 来源: 题型:实验探究题
| 实验步骤 | 实验现象 | 结论 |
| 1.取样,向其中滴加过量的CaCl2(或BaCl2)溶液,过滤 | 产生白色沉淀 | 猜想3成立 |
| 2.向上述滤液中滴加几滴无色酚酞溶液 | 溶液变红 |
查看答案和解析>>
科目: 来源: 题型:实验探究题
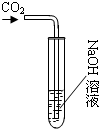 化学学习小组的同学们在探究氢氧化钠的性质时,将二氧化碳通入盛有氢氧化钠溶液的大试管中,如图所示,结果同学们没有观察到明显现象,于是他们展开了如下探究.
化学学习小组的同学们在探究氢氧化钠的性质时,将二氧化碳通入盛有氢氧化钠溶液的大试管中,如图所示,结果同学们没有观察到明显现象,于是他们展开了如下探究.| 实验操作 | 实验现象 | 实验结论 |
| ①取一定量大试管中的溶液于试管中,加入足量CaCl2溶液,过滤 ②向滤液滴加适量酚酞 | ①产生白色沉淀 ②溶液变红 | 贝贝的猜想成立 |
查看答案和解析>>
科目: 来源: 题型:实验探究题
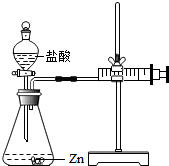 化学兴趣小组的同学对“影响金属与盐酸反应的剧烈程度的因素”进行了探究.
化学兴趣小组的同学对“影响金属与盐酸反应的剧烈程度的因素”进行了探究.| 实验编号 | 选用金属(均取2g) | 盐酸质量分数(均取50mL) | 每分钟产生氢气的体积/mL | |||||
| 1分钟 | 1-2分钟 | 2-3分钟 | 3-4分钟 | 4-5分钟 | 前5分钟共收集气体 | |||
| Ⅰ | 锌片 | 15% | 2.9 | 16.9 | 11.0 | 9.2 | 7.6 | 48.5 |
| Ⅱ | 锌片 | 5% | 1.6 | 8.4 | 5.9 | 4.8 | 3.7 | 24.4 |
查看答案和解析>>
科目: 来源: 题型:计算题
查看答案和解析>>
科目: 来源: 题型:实验探究题
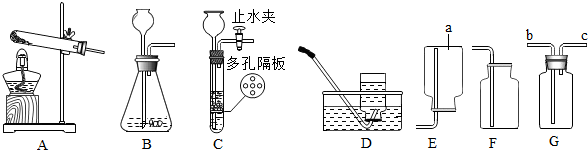
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| 物质 | a | b | c | d |
| 反应前 | 40g | 40g | 0 | 10 |
| 反应中 | 32g | 24g | 24g | ① |
| 反应后 | ② | 0 | ③ | ④ |
| A. | 该反应类型为化合反应 | B. | 反应中a和c的质量比为1:3 | ||
| C. | ②为20g | D. | ③为64g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com