
科目: 来源: 题型:选择题
| A. | x:y=1:1 | B. | x:y=1:2 | C. | x:y=1:4 | D. | x:y=2:1 |
查看答案和解析>>
科目: 来源: 题型:实验探究题

查看答案和解析>>
科目: 来源: 题型:解答题
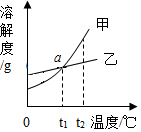 水是生命之源,也是一种重要的资源,日常生活、工农业生产和科学实验都离不开水,请回答下列问题:
水是生命之源,也是一种重要的资源,日常生活、工农业生产和科学实验都离不开水,请回答下列问题:查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| 选项 | 实验目的 | 实验方案 |
| A | 除去铁粉中混有的少量银粉 | 用足量的稀盐酸溶解后过滤 |
| B | 除去二氧化碳中的少量一氧化碳 | 通过灼热的氧化铜 |
| C | 证明分子在不断运动 | 将一滴红墨水滴入一杯纯净水中 |
| D | 收集二氧化碳时,检验集气瓶是否集满 | 用一根燃着的木条放在集气瓶口 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:实验探究题
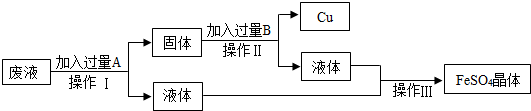
查看答案和解析>>
科目: 来源: 题型:实验探究题

查看答案和解析>>
科目: 来源: 题型:填空题
 用如图装置完成以下实验:
用如图装置完成以下实验:查看答案和解析>>
科目: 来源: 题型:填空题
 ”均为铜片),只需完成实验B和D即可达到探究目的(填字母).
”均为铜片),只需完成实验B和D即可达到探究目的(填字母).
查看答案和解析>>
科目: 来源: 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com