
科目: 来源: 题型:实验探究题
 某学习小组在如图所示的化学药品柜中发现一瓶标签模糊不清的无色溶液,已知这瓶溶液是以下5瓶溶液中的一种:HNO3溶液、Al(NO3)3溶液、Ba(NO3)2溶液、Fe(NO3)2溶液、AgNO3溶液.
某学习小组在如图所示的化学药品柜中发现一瓶标签模糊不清的无色溶液,已知这瓶溶液是以下5瓶溶液中的一种:HNO3溶液、Al(NO3)3溶液、Ba(NO3)2溶液、Fe(NO3)2溶液、AgNO3溶液.| 实验操作 | 预期现象与结论 |
| 1 | 实验现象:溶液变浑浊; 实验结论:是硝酸银溶液 |
| 2 | 实验现象:产生白色沉淀; 实验结论:是硝酸钡溶液 |
查看答案和解析>>
科目: 来源: 题型:实验探究题

查看答案和解析>>
科目: 来源: 题型:实验探究题
查看答案和解析>>
科目: 来源: 题型:实验探究题
| 编号 | 温度/℃ | 加入某盐 | H2SO4体积/mL | H2O体积/mL | 铝粉加入量/g | 铝粉溶解量/g |
| ① | 20 | 不加 | 40 | 0 | 2.0050 | 0.0307 |
| ② | 80 | 不加 | 40 | 0 | 2.0050 | 0.1184 |
| ③ | t1 | 不加 | 20 | V1 | 2.0050 | \ |
| ④ | t2 | 49% CuSO4溶液 | 20 | V2 | 2.0050 | \ |
查看答案和解析>>
科目: 来源: 题型:实验探究题
 一些物质的溶解度曲线如图所示,回答下列问题.
一些物质的溶解度曲线如图所示,回答下列问题.查看答案和解析>>
科目: 来源: 题型:实验探究题
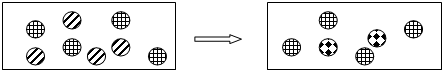
 Na+;
Na+; CO32-;
CO32-; OH-.
OH-.查看答案和解析>>
科目: 来源: 题型:选择题
| 实验操作 | 现象 | 结论 | |
| A | 用拇指堵住收集了甲烷的试管口,靠近火焰,移开拇指点火 | 发出轻微爆鸣声 | 试管中气体为纯净物 |
| B | 往装有某溶液的试管中滴加稀硫酸 | 产生白色沉淀 | 一定含有Ba2+ |
| C | 把燃着的木条插入某瓶无色气体中 | 木条熄灭 | 该瓶中气体不一定是二氧化碳 |
| D | 在燃烧匙里放少量硫,加热,直到发生燃烧,然后把它伸进充满氧气的集气瓶中 | 硫在空气中燃烧发出淡蓝色火焰,而在氧气中燃烧更旺,发出蓝紫色火焰 | 氧气的浓度越小,燃烧越 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| 物 质 | 所含杂质 | 除去杂质的试剂或方法 | |
| A | CO | CO2 | 足量NaOH溶液 |
| B | KCl | KClO3 | MnO2,加热 |
| C | NaCl | Na2CO3 | 过量盐酸,蒸发 |
| D | O2 | H2O | 浓硫酸,干燥 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
 如图所示,在小烧杯乙和丙中分别放入不同的物质后,立即用大烧杯甲罩住小烧杯乙和丙.下列有关现象或结论的说法错误的是( )
如图所示,在小烧杯乙和丙中分别放入不同的物质后,立即用大烧杯甲罩住小烧杯乙和丙.下列有关现象或结论的说法错误的是( )| A. | 乙:浓氨水 丙:紫色石蕊试液. 现象:丙中石蕊试液变蓝 | |
| B. | 乙:浓盐酸 丙:无色酚酞试液. 现象:丙中酚酞试液不变色 | |
| C. | 乙:浓硫酸 丙:硝酸钡溶液. 现象:丙中产生白色沉淀 | |
| D. | 乙:水 丙:浓硫酸.结论:丙中溶质质量分数会减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com