
科目: 来源: 题型:填空题
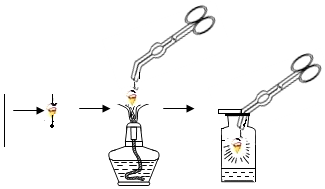 如图所示,为铁丝在氧气中燃烧实验,试回答:
如图所示,为铁丝在氧气中燃烧实验,试回答:查看答案和解析>>
科目: 来源: 题型:实验探究题
| 实验 | 现象 | 解释与结论 |
| 实验1:取直径0.20mm、含碳0.1%的铁丝,在氧气中燃烧 | 零星的火星四射 | ①铁燃烧的文字表达式是铁+氧气$\stackrel{点燃}{→}$四氧化三铁 ②0.20mm的铁丝在氧气中燃烧,“火星四射”与其含碳量的关系为含碳量越高,火星四射的现象越明显 |
| 实验2:取直径0.20mm、含碳0.32%的铁丝,在氧气中燃烧 | 较明显的火星四射 | |
| 实验3:取直径0.20mm、含碳0.52%的铁丝,在氧气中燃烧 | 明显的火星四射 |
查看答案和解析>>
科目: 来源: 题型:实验探究题
查看答案和解析>>
科目: 来源: 题型:推断题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:实验探究题
| 实验装置 | 实验主要过程 |
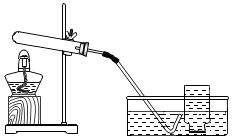 | ①检验装置气密性.操作如下:先将导管伸入液面下,用手紧握试管,观察到,松开手后,导管口有液面上升. ②加入过氧化钙,加热,导管口有大量气泡生成. ③收集满一瓶气体. ④停止加热.熄灭酒精灯前,应先将导管从水槽中移出. ⑤检验气体.方法是将一根带火星的木条伸进集气瓶内,如果木条复燃,说明该瓶内的气体是氧气. |
| 实验装置 | 实验主要过程 |
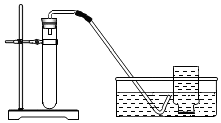 | ①检验装置气密性. ②加入过氧化钙和水后,有少量细小气泡缓慢放出,在导管口几乎收集不到气体.该装置放置到第二天,集气瓶中只收集到极少量气体,振荡试管后仍有少量细小气泡缓慢放出. |
查看答案和解析>>
科目: 来源: 题型:实验探究题
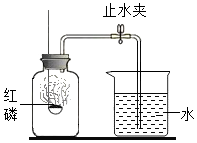 某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下:
某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下:查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com