
科目: 来源: 题型:实验探究题
 甲、乙两同学在学完酸的化学性质后,做了如下实验:
甲、乙两同学在学完酸的化学性质后,做了如下实验:查看答案和解析>>
科目: 来源: 题型:解答题
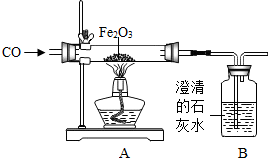 化学兴趣小组的同学设计了用一氧化碳气体还原氧化铁的实验装置,如图所示.请回答下列问题:
化学兴趣小组的同学设计了用一氧化碳气体还原氧化铁的实验装置,如图所示.请回答下列问题:查看答案和解析>>
科目: 来源: 题型:计算题
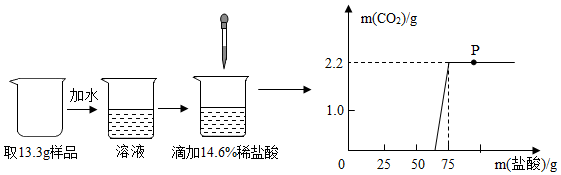
查看答案和解析>>
科目: 来源: 题型:实验探究题
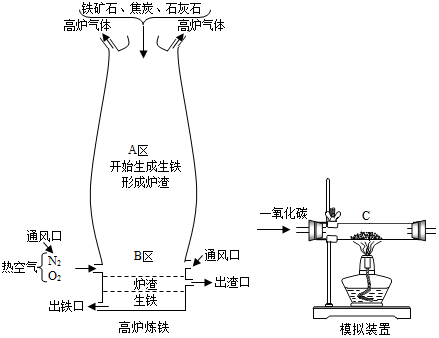
| 物质 | 四氧化三铁 | 氧化亚铁 | 铁粉 |
| 颜色 | 黑色 | 黑色 | 黑色 |
| 能否被磁铁吸引 | 能 | 不能 | 能 |
| 与盐酸反应溶液颜色 | 黄色 | 浅绿色 | 浅绿色 |
| 实验方法 | 实验操作 | 预期现象 | 结论 |
| 物理方法 | 步骤1 | 黑色粉末全部被吸引 | 猜想②成立 |
| 化学方法 | 步骤2 | 产生气泡,溶液变成黄色 |
查看答案和解析>>
科目: 来源: 题型:填空题
 能与对面
能与对面 中能反应的为同伴,硫酸找同伴1,同伴1找同伴2,同伴2找同伴3,见图.
中能反应的为同伴,硫酸找同伴1,同伴1找同伴2,同伴2找同伴3,见图.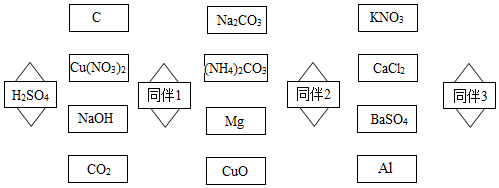
查看答案和解析>>
科目: 来源: 题型:解答题
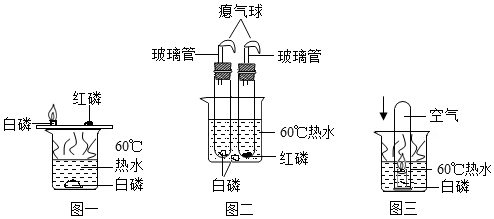
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 受热时水分子的体积逐渐变大 | |
| B. | 化学变化时水分子的性质不变 | |
| C. | 结冰时水分子间的间隔变大 | |
| D. | 反应时构成水分子的原子种类发生改变 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com