
科目: 来源: 题型:实验探究题
| 实验编号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 二氧化锰的质量(g) | 0.1 | 0.2 | 0.33 | 0.4 | 0.5 | 0.66 | 1 | 1.3 | 2 | 3 |
| 二氧化锰与氯酸钾的质量比 | 1:20 | 1:10 | 1:6 | 1:5 | 1:4 | 1:3 | 1:2 | 2:3 | 1:1 | 3:2 |
| 生成200ml氧气时间(秒) | 235 | 186 | 162 | 147 | 133 | 117 | 143 | 160 | 211 | 244 |
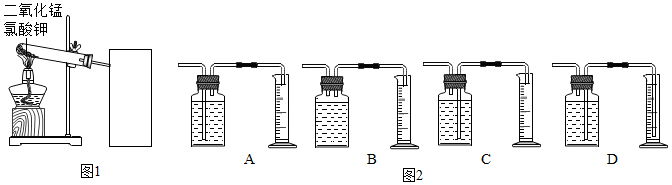
查看答案和解析>>
科目: 来源: 题型:实验探究题

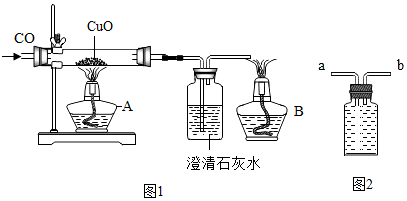
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:实验探究题
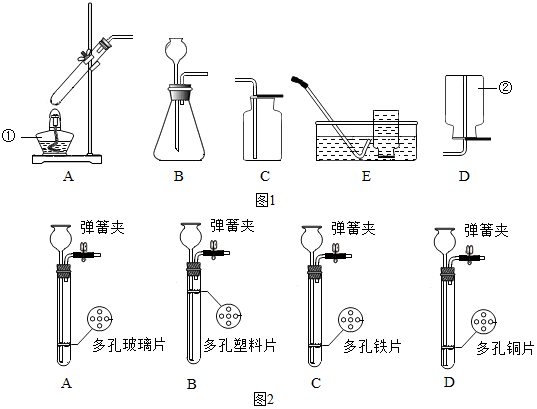
| 气体 性质 | 氢气 | 二氧化碳 | 二氧化硫 |
| 密度(g•L-1) | 0.08987 | 1.975 | 2.716 |
| 溶解程度 | 极难溶于水 | 能溶于水 | 易溶于水 |
查看答案和解析>>
科目: 来源: 题型:填空题
 我国使用“长征二号F”运载火箭将“神州十一”送上轨道,并与天宫一号成功对接.运载火箭由三级火箭组成.一级和二级火箭的推进物(燃料)为偏二甲肼(化学式:C2H8N2)和四氧化二氮,在点火后,反应生成水、氮气和一种空气中常见的气体;在反应的过程中四氧化二氮不稳定,易分解成NO2,所以火箭点火后往往看到大量棕烟雾.三级火箭的推进物为液氢和液氧.
我国使用“长征二号F”运载火箭将“神州十一”送上轨道,并与天宫一号成功对接.运载火箭由三级火箭组成.一级和二级火箭的推进物(燃料)为偏二甲肼(化学式:C2H8N2)和四氧化二氮,在点火后,反应生成水、氮气和一种空气中常见的气体;在反应的过程中四氧化二氮不稳定,易分解成NO2,所以火箭点火后往往看到大量棕烟雾.三级火箭的推进物为液氢和液氧.查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:选择题
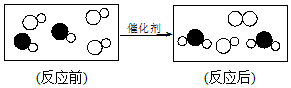 如图是“尾气催化转换器”将汽车尾气中有毒气体转变为无毒气体的微观示意图,其中不同的园球代表不同原子.下列说法错误的是( )
如图是“尾气催化转换器”将汽车尾气中有毒气体转变为无毒气体的微观示意图,其中不同的园球代表不同原子.下列说法错误的是( )| A. | 参加反应的两种分子的个数比为1:1 | |
| B. | 原子在化学变化中是不可分的 | |
| C. | 图中生成物全部是化合物 | |
| D. | 此反应有单质生成 |
查看答案和解析>>
科目: 来源: 题型:选择题
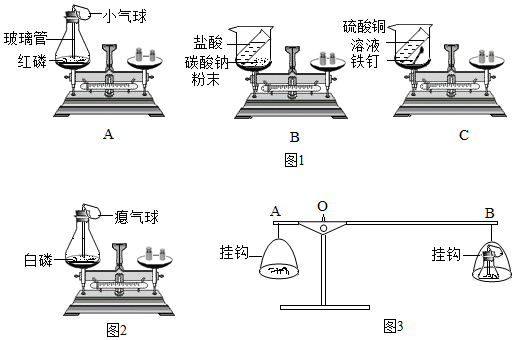
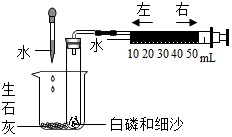 某化学小组利用如图所示实验装置测定空气中氧气的含量(部分固定装置已略去).关于该实验有下列说法:①向烧杯中加水是为了提高烧杯内的温度;②白磷燃烧会放出大量的白雾;③白磷的量不足,会使测定的结果偏大;④实验中可观察到,注射器的活塞先向右移动,后向左移动;⑤若试管内净容积为50mL,反应后冷却至室温,活塞停止在40mL附近.其中正确的是( )
某化学小组利用如图所示实验装置测定空气中氧气的含量(部分固定装置已略去).关于该实验有下列说法:①向烧杯中加水是为了提高烧杯内的温度;②白磷燃烧会放出大量的白雾;③白磷的量不足,会使测定的结果偏大;④实验中可观察到,注射器的活塞先向右移动,后向左移动;⑤若试管内净容积为50mL,反应后冷却至室温,活塞停止在40mL附近.其中正确的是( )| A. | ①②③ | B. | ②③⑤ | C. | ③④⑤ | D. | ①④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com