
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 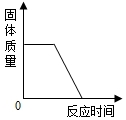 加热一定质量的高锰酸钾 | |
| B. | 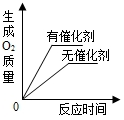 用等质量、等质量分数的双氧水制取氧气 | |
| C. | 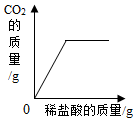 向一定质量的大理石(杂质不参加反应)中滴加稀盐酸 | |
| D. | 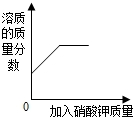 某温度,向一定量饱和硝酸钾溶液中加人硝酸钾晶体 |
查看答案和解析>>
科目: 来源: 题型:选择题
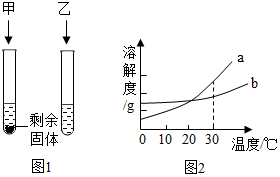 10℃时,向两只试管中加入等质量的甲、乙两种固体物质,分别加入10g水,使其充分溶解,观察到如图1所示的现象.图2是甲、乙两种物质的溶解度曲线.下列说法错误的是( )
10℃时,向两只试管中加入等质量的甲、乙两种固体物质,分别加入10g水,使其充分溶解,观察到如图1所示的现象.图2是甲、乙两种物质的溶解度曲线.下列说法错误的是( )| A. | 10℃时,甲一定是饱和溶液 | |
| B. | 10℃时,乙一定是不饱和溶液 | |
| C. | 给两支试管加热至30℃,甲、乙溶液的溶质质量分数相等 | |
| D. | 30℃时,将两支试管溶液制成饱和溶液,则它们的质量:甲>乙 |
查看答案和解析>>
科目: 来源: 题型:选择题
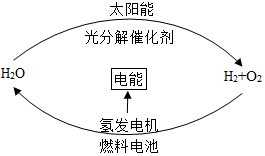 对于如图的说法中,错误的是( )
对于如图的说法中,错误的是( )| A. | 燃料电池能够使化学反应产生的能量转化为电能 | |
| B. | 该氢能源的循环体系能够实现太阳能转化为电能 | |
| C. | 在此循环中发生了反应:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑ | |
| D. | 目前化学家急需解决的问题是寻找更加合适的催化剂 |
查看答案和解析>>
科目: 来源: 题型:解答题
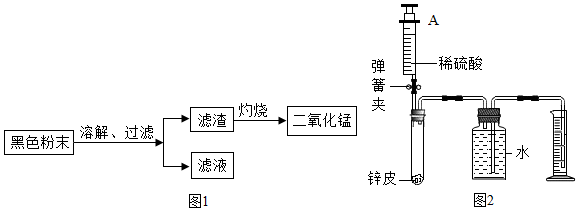
查看答案和解析>>
科目: 来源: 题型:实验探究题
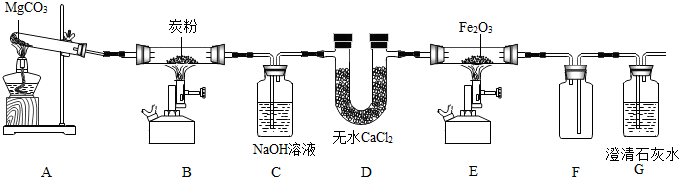
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com