
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题

| A. | 变红色 | B. | 变蓝色 | C. | 变白色 | D. | 不变色 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 雾霾与空气污染有关 | |
| B. | 废旧电池应埋入地下 | |
| C. | 化石燃料的燃烧会造成空气污染 | |
| D. | 汽车改用压缩天然气,可以减少汽车尾气的污染 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:实验探究题
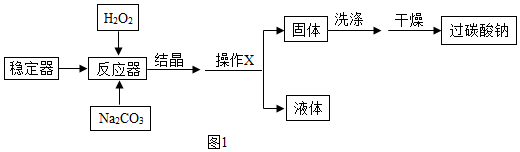
 小明同学新买了一台氧立得便携式制氧器,其中有A、B两包固体,B包为黑色固体粉未,经查阅资料知A包主要成分为过碳酸钠.将A包、B包药品分别放入机器,就可以制得氧气.为探究A包固体的纯度,设计了如图2所示实验装置.
小明同学新买了一台氧立得便携式制氧器,其中有A、B两包固体,B包为黑色固体粉未,经查阅资料知A包主要成分为过碳酸钠.将A包、B包药品分别放入机器,就可以制得氧气.为探究A包固体的纯度,设计了如图2所示实验装置.查看答案和解析>>
科目: 来源: 题型:实验探究题

查看答案和解析>>
科目: 来源: 题型:实验探究题
 纳米铁粉在空气中不自燃,稍加热即剧烈燃烧,某化学兴趣小组设计如图所
纳米铁粉在空气中不自燃,稍加热即剧烈燃烧,某化学兴趣小组设计如图所查看答案和解析>>
科目: 来源: 题型:解答题
 溶解是生活中常见的现象,不同物质在水中的溶解能力不同.
溶解是生活中常见的现象,不同物质在水中的溶解能力不同.| 温度(℃) | 0 | 20 | 30 | 40 | 60 |
| KNO3 | 13.3 | 31.6 | 45.8 | 63.9 | 110 |
| NaCl | 35.7 | 36.0 | 36.3 | 36.6 | 37.3 |
查看答案和解析>>
科目: 来源: 题型:推断题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 根据纯净物中元素的种类数,将其分为单质与化合物 | |
| B. | 根据一定温度下溶液能否再溶解溶质,将其分为饱和溶液与不饱和溶液 | |
| C. | 根据离子的电性,将其分为阳离子与阴离子 | |
| D. | 根据溶质的多少,将溶液分为浓溶液和稀溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com