
科目: 来源: 题型:计算题
查看答案和解析>>
科目: 来源: 题型:解答题
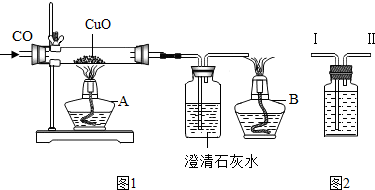 课题式课堂教学是探究学习的一种方式,其基本教学模式为:提出课题→确定研究方案→解决问题→总结和评价.图1是关于《一氧化碳的化学性质》的课题式课堂教学中,在解决问题阶段甲同学设计的证明CO具有还原性的实验装置,装置气密性良好.
课题式课堂教学是探究学习的一种方式,其基本教学模式为:提出课题→确定研究方案→解决问题→总结和评价.图1是关于《一氧化碳的化学性质》的课题式课堂教学中,在解决问题阶段甲同学设计的证明CO具有还原性的实验装置,装置气密性良好.查看答案和解析>>
科目: 来源: 题型:选择题
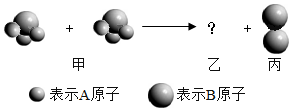 如图所示,两个甲分子反应生成三个乙分子一个丙分子,则从图示获得的信息中,不正确的是( )
如图所示,两个甲分子反应生成三个乙分子一个丙分子,则从图示获得的信息中,不正确的是( )| A. | 分子的种类在化学反应中发生了改变 | |
| B. | 该反应的反应类型为分解反应 | |
| C. | 反应生成的丙物质属于单质 | |
| D. | 一个丙分子由两个B原子组成 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 延展性 | B. | 导热性 | C. | 弹性 | D. | 导电性 |
查看答案和解析>>
科目: 来源: 题型:解答题
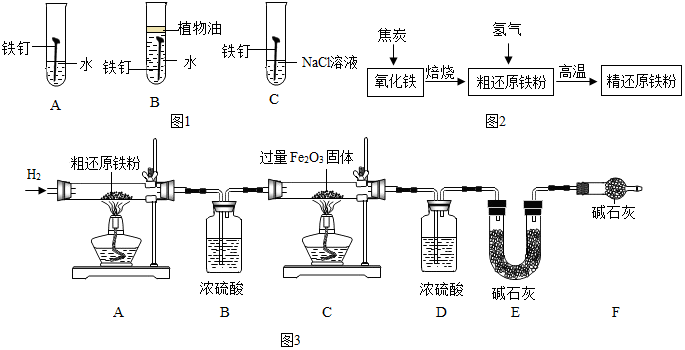
查看答案和解析>>
科目: 来源: 题型:解答题
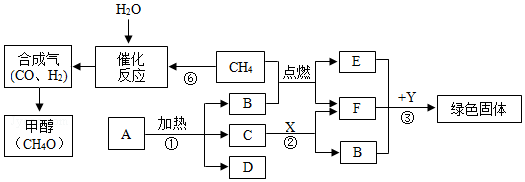
查看答案和解析>>
科目: 来源: 题型:推断题
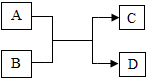 如图所示A、B 在一定条件下转化为C、D.
如图所示A、B 在一定条件下转化为C、D.查看答案和解析>>
科目: 来源: 题型:实验探究题
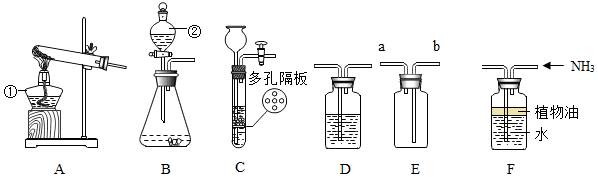
查看答案和解析>>
科目: 来源: 题型:多选题
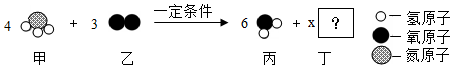
| A. | 反应前后,分子种类不变 | |
| B. | x=2,丁为N2 | |
| C. | 丙、丁的质量比为9:14 | |
| D. | 改变反应条件,反应中乙、丙化学计量数之比为5:6,则丁的化学式为NO2 |
查看答案和解析>>
科目: 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com