
科目: 来源: 题型:多选题
 现有两种金属单质组成的混合物.向100g某稀盐酸(足量)中加入该混合物,混合物的质量与生成氢气的质量关系如图所示.下列说法正确的是( )(填序号)
现有两种金属单质组成的混合物.向100g某稀盐酸(足量)中加入该混合物,混合物的质量与生成氢气的质量关系如图所示.下列说法正确的是( )(填序号)| A. | 若混合物为Zn、Al,则m可能是0.2 | |
| B. | 若混合物为Zn、Cu,则m可能是0.2 | |
| C. | 若混合物为Fe、Al,则稀盐酸中溶质质量分数可能是7.3% | |
| D. | 若混合物为Fe、Cu,m为0.1 g,则该混合物中Fe的质量分数一定是50% |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 79.5% | B. | 53% | C. | 80% | D. | 92.5% |
查看答案和解析>>
科目: 来源: 题型:解答题
| 一 | 二 | 三 | 四 | |
| 加入黄铜样品质量/g | 1 | 2 | 3 | 4 |
| 生成氢气的质量/g | 0.02 | 0.04 | 0.05 | M |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
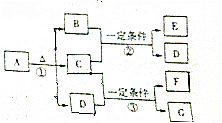 A-G7种物质之间的转化关系如图所示,且B、C、G在常温下是气体,D是液体,E、F是有机物,F的相对分子质量是E的3倍.A的相对分子质量是79.E中的4种元素的原子个数比为1:1:2:4
A-G7种物质之间的转化关系如图所示,且B、C、G在常温下是气体,D是液体,E、F是有机物,F的相对分子质量是E的3倍.A的相对分子质量是79.E中的4种元素的原子个数比为1:1:2:4查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:填空题
 已知A、B、C、D、E、F均为初中化学常见的物质.其中“-”表示相述的物质间能发生化学反应“→”表示转化,A和水反应转化为B,C在潮湿的空气中可以反应产生D,E为含有钠离子的一种盐,F可用硝酸银溶液和稀硝酸来检验,根据如图所示的转化关系,回答下列问题.(图中反应条件均已略去,反应物和产物均已给出)
已知A、B、C、D、E、F均为初中化学常见的物质.其中“-”表示相述的物质间能发生化学反应“→”表示转化,A和水反应转化为B,C在潮湿的空气中可以反应产生D,E为含有钠离子的一种盐,F可用硝酸银溶液和稀硝酸来检验,根据如图所示的转化关系,回答下列问题.(图中反应条件均已略去,反应物和产物均已给出)查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com