
科目: 来源: 题型:实验探究题

查看答案和解析>>
科目: 来源: 题型:填空题
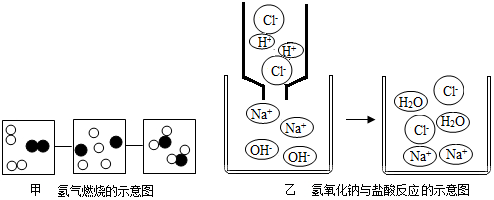
查看答案和解析>>
科目: 来源: 题型:实验探究题
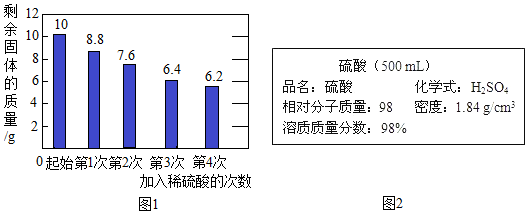
查看答案和解析>>
科目: 来源: 题型:实验探究题
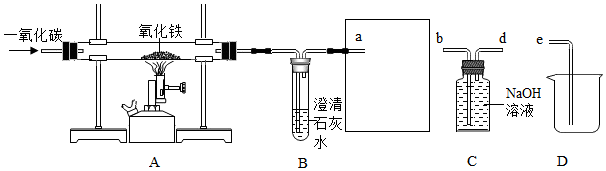
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 一定有C、H、O三种元素 | |
| B. | 只含有C、H两种元素 | |
| C. | 一定有C、H两种元素,可能含有O元素 | |
| D. | C、H两种元素质量比为11:9 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 镉>铜>X | B. | 铜>镉>X | C. | X>铜>镉 | D. | 镉>X>铜 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 湖南某些厂加工的劣质奶粉是用淀粉、蔗糖、奶香精等掺和成的 | |
| B. | 某些地方工厂用工业石蜡等给 瓜子“打蜡美容” | |
| C. | 在天津市发现的“注胶虾” | |
| D. | 用硫磺燃烧法熏蒸粉丝 |
查看答案和解析>>
科目: 来源: 题型:解答题
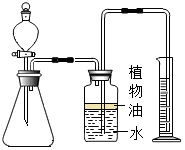 氮化铝(AlN)是一种新型无机材料,某氮化铝样品中含有碳或氧化铝杂质.已知:①氮化铝和NaOH溶液能反应,其反应方程式为:AlN+NaOH+H2O=NaAlO2+NH3↑②氧化铝也能与氢氧化钠溶液反应而全部溶解,但不生成气体.小黄用如图所示中的一些装置来进行相关实验,根据反应中所生成氨气的体积来测定样品中的氮化铝的质量分数,并根据实验现象来确定杂质的成分(实验中导管体积忽略不计).
氮化铝(AlN)是一种新型无机材料,某氮化铝样品中含有碳或氧化铝杂质.已知:①氮化铝和NaOH溶液能反应,其反应方程式为:AlN+NaOH+H2O=NaAlO2+NH3↑②氧化铝也能与氢氧化钠溶液反应而全部溶解,但不生成气体.小黄用如图所示中的一些装置来进行相关实验,根据反应中所生成氨气的体积来测定样品中的氮化铝的质量分数,并根据实验现象来确定杂质的成分(实验中导管体积忽略不计).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com