
科目: 来源: 题型:实验探究题
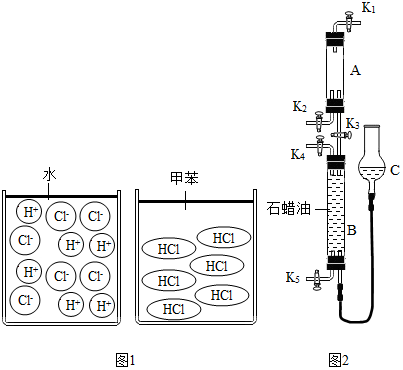
| 实验内容 | 实验现象 | 解释与结论 |
| 测定导电性 | 氯化氢的水溶液:导电性良好 | 氯化氢的水溶液中有自由移动的离子 |
| 氯化氢的甲苯溶液:不导电 | 氯化氢的甲苯溶液没有自由移动的离子 | |
| 与镁作用 | 氯化氢的水溶液:有气泡产生 | 化学方程式:Mg+2HCl═MgCl2+H2↑ |
| 氯化氢的甲苯溶液:没有明显现象 | 氯化氢的甲苯溶液没有解离出氢离子 | |
| 与固态碳酸钠作用 | 氯化氢的水溶液:产生气泡 | 化学方程式Na2CO3+2HCl=2NaCl+H2O+CO2↑ |
| 氯化氢的甲苯溶液:没有气泡产生 | 氯化氢的甲苯溶液没有解离出氢离子 |
查看答案和解析>>
科目: 来源: 题型:填空题
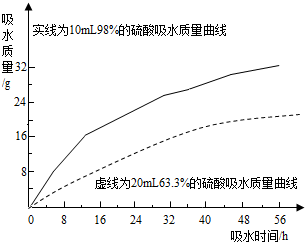 硫酸是常见的酸,也是常用的化工原料.由于浓度不同,浓硫酸与稀硫酸在性质上存在较大差异,如浓硫酸具有脱水性、吸水性和强腐蚀性等.某课外兴趣小组为了探究浓硫酸的某些特性做了如下一些实验.请结合有关实验,按要求回答下列问题:
硫酸是常见的酸,也是常用的化工原料.由于浓度不同,浓硫酸与稀硫酸在性质上存在较大差异,如浓硫酸具有脱水性、吸水性和强腐蚀性等.某课外兴趣小组为了探究浓硫酸的某些特性做了如下一些实验.请结合有关实验,按要求回答下列问题:| 方案 | 实验假设 | 实验方案 | 实验现象与结论 |
| Ⅰ | 能发生钝化 | 取一铁片先插入浓硫酸中,一段时间后取出,再插入硫酸铜溶液中. | 无明显变化,假设成立. |
| Ⅱ | 能发生钝化 | 取两片相同的铁片,一片放入浓硫酸中,一段时间后取出,与另一片同时放入硫酸铜溶液中. | 浸过浓硫酸的铁片表面无明显变化,另一铁片表面产生红色固体,假设成立. |
查看答案和解析>>
科目: 来源: 题型:实验探究题
 某校研究性学习小组用如图装置进行镁条在空气中燃烧实验.当燃烧停止,冷却后打开止水夹,进入集气瓶的水体积约占集气瓶体积的70%,请回答:
某校研究性学习小组用如图装置进行镁条在空气中燃烧实验.当燃烧停止,冷却后打开止水夹,进入集气瓶的水体积约占集气瓶体积的70%,请回答:查看答案和解析>>
科目: 来源: 题型:实验探究题

查看答案和解析>>
科目: 来源: 题型:选择题
| A. | a、b、c三种酸溶液中的H原子数目:c>a>b | |
| B. | a、b、c的相对分子质量:b<a<c | |
| C. | a、b、c与金属Mg反应的速率:b>a>c | |
| D. | a、b、c可能分别为H2Y、HX、H3Z |
查看答案和解析>>
科目: 来源: 题型:计算题
查看答案和解析>>
科目: 来源: 题型:实验探究题

查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题
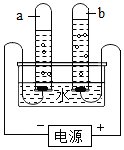 实验是化学学习的一种重要手段,如利用电解水实验可探究水的组成.请根据电解水实验回答下列问题:
实验是化学学习的一种重要手段,如利用电解水实验可探究水的组成.请根据电解水实验回答下列问题:| 时间/分钟 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 阴极生成气体体积(cm3) | 6 | 12 | 20 | 29 | 39 | 49 | 55 | 65 | 75 | 85 |
| 阳极生成气体体积(cm3) | 2 | 4 | 7 | 11 | 16 | 21 | 26 | 31 | 36 | 41 |
查看答案和解析>>
科目: 来源: 题型:填空题
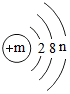 ,请回答下列问题:
,请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com