
科目: 来源: 题型:选择题
| A. | 碳在空气中充分燃烧 2C+O2$\frac{\underline{\;点燃\;}}{\;}$2CO | |
| B. | 铁钉浸入硫酸铜溶液中 2Fe+3CuSO4═3Cu+Fe2(SO4)3 | |
| C. | 镁带燃烧 Mg+O2$\frac{\underline{\;点燃\;}}{\;}$MgO2 | |
| D. | 红磷燃烧 4P+5O2 $\frac{\underline{\;点燃\;}}{\;}$2P2O5 |
查看答案和解析>>
科目: 来源: 题型:实验探究题
 如图所示实验台上有一瓶标签残缺的试剂,同学们对此进行了如下探究:
如图所示实验台上有一瓶标签残缺的试剂,同学们对此进行了如下探究:| 甲同学 | 乙同学 | 丙同学 | |
| 实验方案 | 测溶液pH | 滴加无色酚酞溶液 | 滴加BaCl2溶液 |
| 实验操作 | 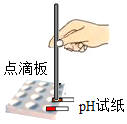 | 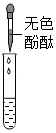 | 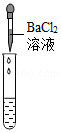 |
| 实验现象 | 试纸不变色,对比标准的比色卡,pH=7 | 溶液变红 | 产生白色沉淀 |
| 实验方程式 | Na2CO3+BaCl2=BaCO3↓+2NaCl | ||
| 实验结论 | 甲同学猜想成立 | 乙同学猜想成立 | 丙同学猜想成立 |
查看答案和解析>>
科目: 来源: 题型:实验探究题
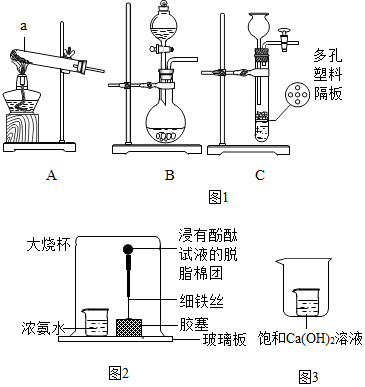
查看答案和解析>>
科目: 来源: 题型:实验探究题
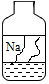 同学们在初中化学实验室中发现一瓶久置的、瓶口有白色固体、瓶塞丢失的无色溶液,如图所示.已知原溶液可能是NaCl、NaOH或Na2CO3三种溶液中的一种,为确定该溶液的成分,同学们进行了如下探究:
同学们在初中化学实验室中发现一瓶久置的、瓶口有白色固体、瓶塞丢失的无色溶液,如图所示.已知原溶液可能是NaCl、NaOH或Na2CO3三种溶液中的一种,为确定该溶液的成分,同学们进行了如下探究:查看答案和解析>>
科目: 来源: 题型:实验探究题

| 仪器编号 | 所盛试剂的名称 | 试剂或装置的作用 |
| A | 澄清石灰水 | 证明二氧化碳的存在 |
| B | 浓硫酸 | 吸收水煤气中的水蒸气 |
| C | 因为氢气燃烧生成水,看到烧杯内壁上有水珠出现,能证明H2存在 | |
| D | 一氧化碳燃烧生成二氧化碳,二氧化碳能使澄清石灰水变浑浊能证明CO存在 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 用酒精灯加热试管里的液体时,试管里的液体不应超过试管容积的$\frac{2}{3}$ | |
| B. | 实验后剩余的药品应放回原试剂瓶中,避免浪费 | |
| C. | 洗过的玻璃仪器内壁附着的水滴既不聚成水滴,也不成股流下时,表明仪器已洗干净 | |
| D. | 不小心碰倒酒精灯,洒出的酒精在桌上燃烧起来时,应立即用水扑灭 |
查看答案和解析>>
科目: 来源: 题型:选择题
| 选项 | 鉴别的物质 | 鉴别的方法 |
| A | 纯水和矿泉水 | 观察是否澄清 |
| B | 硬水和软水 | 加肥皂水,振荡,观察泡沫的多少 |
| C | 水和过氧化氢溶液 | 加二氧化锰,观察是否有气泡 |
| D | 二氧化碳和氮气 | 加澄清石灰水,振荡,观察是否变浑浊 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:实验探究题
 干冰是固态的二氧化碳,在常温下易升华,如图是干冰升华时的情景,根据图中信息,从“物质性质$?_{反映}^{决定}$物质用途”这一角度分析干冰具有的性质和用途.
干冰是固态的二氧化碳,在常温下易升华,如图是干冰升华时的情景,根据图中信息,从“物质性质$?_{反映}^{决定}$物质用途”这一角度分析干冰具有的性质和用途.查看答案和解析>>
科目: 来源: 题型:实验探究题
 请结合下列实验常用装置,回答有关问题.
请结合下列实验常用装置,回答有关问题.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com