
科目: 来源: 题型:实验探究题
| 实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| H2O2溶液溶质质量分数 | 1% | 3% | 5% | 10% | 15% | 20% | 25% | 30% |
| MnO2粉末用量(g) | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 |
| 收集一瓶气体时所用时间(秒) | 660 | 220 | 205 | 80 | 25 | 9 | 4 | 3 |
| 反应后液体温度(℃) | 24 | 34 | 39 | 56 | 65 | 67 | 69 | 70 |
| 实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| MnO2粉末用量(g) | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 | 0.6 | 0.7 | 0.8 | 0.9 | 1.0 |
| 所用时间(秒) | 17 | 8 | 7 | 5 | 4 | 3 | 2 | 2 | 2 | 2 |
查看答案和解析>>
科目: 来源: 题型:实验探究题
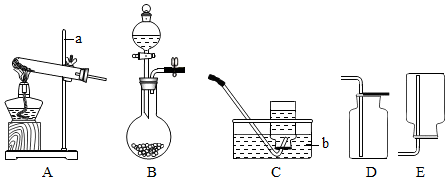
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ②或③ | B. | ①或③ | C. | ①②③均可 | D. | 无法确定 |
查看答案和解析>>
科目: 来源: 题型:实验探究题
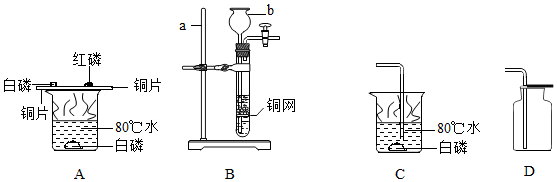
查看答案和解析>>
科目: 来源: 题型:实验探究题
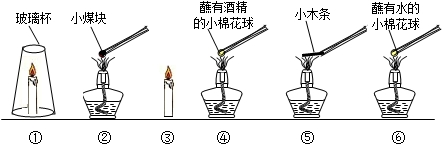
| 实验假设 | 实验内容 | 实验现象 | 实验结论 |
| 1.可能与物质性质有关; | [实验1]:(实验装置应选择 ④⑥;) | 燃烧;没有燃烧. | 条件1:物质具有可燃性; |
| 2.可能与是否有氧气有关; | [实验2]:(实验装置应选择 ③①;) | 很快熄灭;持续燃烧 | 条件2:要与氧气接触; |
| 3.可能与与着火点有关. | [实验3]:(实验装置应选择 ⑤②;) | 点燃时间短;点燃时间长; | 条件3:着火点低先燃烧 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | CaO→Ca(NO3)2 | B. | Al(OH)3→Al2(SO4)3 | C. | FeO→FeCl3 | D. | Na2CO3→NaCl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com