
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:推断题

查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:实验探究题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:实验探究题
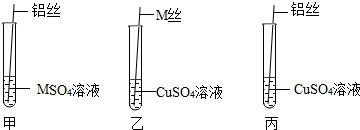
| 实验操作 | 实验想象 | 实验结论 |
| 铝丝插入装有MSO4溶液的试管中(图甲) | 铝丝表面出现一层黑色物质 | Al>M |
| M丝插入装有CuSO4溶液的试管中(图乙) | M丝表面出现一层红色物质,溶液的颜色 由蓝色变为无色. | M>Cu |
| 铝丝插入装有CuSO4溶液的试管中(图丙) | M丝表面出现一层红色物质,颜色由蓝色变为无色 | Al>Cu |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com