
科目: 来源: 题型:选择题
| A. | CO2气体(CO)--点燃 | B. | O2(N2)--通过红热的铜丝 | ||
| C. | CO2气体(H2O)--通过无水氯化钙 | D. | Fe(Cu)--在空气中燃烧 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:计算题

查看答案和解析>>
科目: 来源: 题型:计算题
查看答案和解析>>
科目: 来源: 题型:实验探究题

查看答案和解析>>
科目: 来源: 题型:填空题

查看答案和解析>>
科目: 来源: 题型:推断题
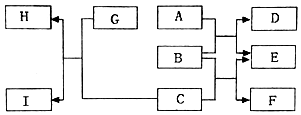 A-I表示初中化学常见的物质,其中,C的浓溶液常用作干燥某些气体,H是最清洁燃料,D是蓝色沉淀,各物质间相互转化关系如图所示,请回答下列问题:
A-I表示初中化学常见的物质,其中,C的浓溶液常用作干燥某些气体,H是最清洁燃料,D是蓝色沉淀,各物质间相互转化关系如图所示,请回答下列问题:查看答案和解析>>
科目: 来源: 题型:选择题
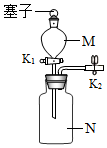
| A. | K2关闭、K1打开、塞子塞紧时,若M中的水不能流下则装置气密性好 | |
| B. | 若M中盛放双氧水,N中盛放二氧化锰,则可以制取氧气 | |
| C. | 若M中盛放稀盐酸,N中盛放块状大理石,则可以制取二氧化碳 | |
| D. | N中储满不溶于水的气体时,将水不断由M注入N中,即可将气体排出 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com