
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
 请同学们搭乘“化学地铁”畅游初中常见物质世界.如图所示,列车上的物质可与各站的对应物质发生反应,方可驶向下一站.“2号站”对应的物质由两种元素组成,“3号站”和“4号站”对应的物质均由三种元素组成且二者能发生化学反应.
请同学们搭乘“化学地铁”畅游初中常见物质世界.如图所示,列车上的物质可与各站的对应物质发生反应,方可驶向下一站.“2号站”对应的物质由两种元素组成,“3号站”和“4号站”对应的物质均由三种元素组成且二者能发生化学反应.查看答案和解析>>
科目: 来源: 题型:解答题
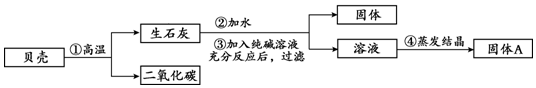
查看答案和解析>>
科目: 来源: 题型:解答题
 阅读下面科普短文.
阅读下面科普短文.查看答案和解析>>
科目: 来源: 题型:解答题
 金属和金属材料在生活中有广泛用途.
金属和金属材料在生活中有广泛用途.查看答案和解析>>
科目: 来源: 题型:解答题
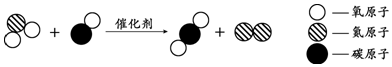
查看答案和解析>>
科目: 来源: 题型:选择题
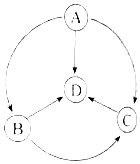 物质之间的相互转化是化学的重要知识.图中箭头表示物质之间可以向箭头方向一步转化,下列说法中不正确的是( )
物质之间的相互转化是化学的重要知识.图中箭头表示物质之间可以向箭头方向一步转化,下列说法中不正确的是( )| A. | 若四种物质均为金属单质,则A的金属活动性最强 | |
| B. | 若四种物质均为含钙化合物,A、C都只含两种元素.B生成D时无气体产生,则C、D属于盐类 | |
| C. | 若A常温下为液体,B、C的组成元素完全相同,D是一种单质,则只有B、C能使紫色石蕊试液变红 | |
| D. | 若图中箭头全部调换方向,A、B的组成元素完全相同,C是一种单质,则D常温下只能为固体或液体 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | X>Y>Z | B. | Y>Z>X | C. | Y>X>Z | D. | X>Z>Y |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com