
科目: 来源: 题型:多选题
| 选项 | 需要鉴别的物质 | 鉴别方法 |
| A | 碳酸钠、氯化钠溶液、氢氧化钠溶液 | 滴加酚酞溶液 |
| B | 氢氧化钠、硝酸铵、碳酸钙 | 加入足量的水 |
| C | 氮气、氧气、二氧化碳 | 用燃着的木条区分 |
| D | 铁粉、木炭粉、氧化铜粉末 | 加入足量的稀硫酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 所有含碳元素的化合物都是有机物 | |
| B. | 草木灰的主要成分是碳酸钾、碳酸钾属于复合肥料 | |
| C. | 做饭时,若燃气灶的火焰呈现黄色,锅底出现黑色,则需要调大灶具的进风口 | |
| D. | 一氧化碳有毒,燃着的煤炉会产生一氧化碳,在煤炉上放一壶水能防止人中毒 |
查看答案和解析>>
科目: 来源: 题型:实验探究题
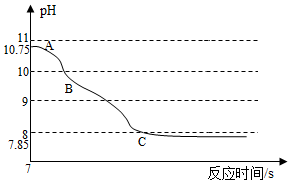 实验室用石灰水而不用氢氧化钠溶液鉴定二氧化碳.氢氧化钠能否与二氧化碳反应?
实验室用石灰水而不用氢氧化钠溶液鉴定二氧化碳.氢氧化钠能否与二氧化碳反应?| 操作 | NaHCO3溶液 | Na2CO3溶液 |
| 加入稀盐酸 | 产生气泡 | 产生气泡 |
| 加入稀CaCl2溶液 | 无明显变化 | 产生白色沉淀(填写现象)) |
| 加热溶液至沸腾,并将气体通入澄清石灰水 | 澄清石灰水变浑浊 | 澄清石灰水无明显变化 |
| 实验操作 | 实验现象 | 结论及化学方程式 |
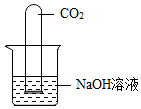 | 试管内液面上升 | 氢氧化钠与二氧化碳反应生成碳酸钠.反应方程式CO2+2NaOH═Na2CO3+H2O |
| 实验步骤 | 实验现象 | 解释与结论 |
| 向溶液中加入足量的稀盐酸 | 产生气泡 | NaOH与CO2发生了反应 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:实验探究题
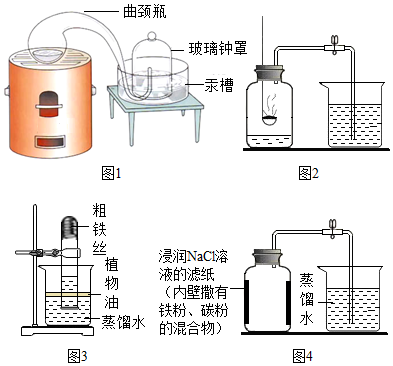
| 实验前的体积 | 实验后的体积 | |
| 集气瓶内空气 | 烧杯内蒸馏水 | 烧杯内剩余蒸馏水 |
| 131mL | 90.0mL | 63.6mL |
查看答案和解析>>
科目: 来源: 题型:解答题
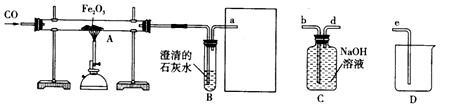
查看答案和解析>>
科目: 来源: 题型:填空题
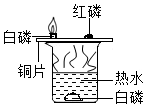 燃烧是人类最早利用的化学反应之一,与人类的生产、生活有密切的联系
燃烧是人类最早利用的化学反应之一,与人类的生产、生活有密切的联系查看答案和解析>>
科目: 来源: 题型:填空题

查看答案和解析>>
科目: 来源: 题型:实验探究题

| 方案编号 | 实验操作 | 实验现象 | 结论 |
| 方案1 | 取样于试管中,滴加紫色石蕊试液 | 溶液变红色 | 猜想a成立 |
| 方案2 | 取样于试管中,滴加硝酸银溶液 | 产生白色沉淀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com