
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
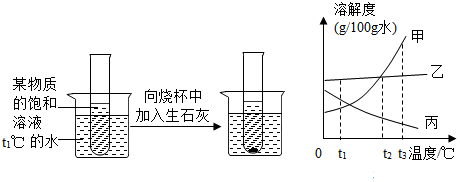
查看答案和解析>>
科目: 来源: 题型:解答题
 水是人类宝贵的自然资源.
水是人类宝贵的自然资源.查看答案和解析>>
科目: 来源: 题型:计算题
查看答案和解析>>
科目: 来源: 题型:填空题
| 主食 | 米饭、馒头 |
| 副食 | 红烧肉、鸡蛋、豆腐汤 |
| 饮料 | 纯净水、可乐 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题
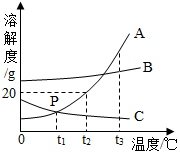 A、B、C三种晶体(不含结晶水)的溶解度曲线如图.,请回答:
A、B、C三种晶体(不含结晶水)的溶解度曲线如图.,请回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com