
科目: 来源: 题型:选择题
| A. | 苏打饼干包装袋内有小袋生石灰,作为补钙剂 | |
| B. | 汽水中含有碳酸,碳酸属于有机物 | |
| C. | 人体中的化学元素分为微量元素和常量元素 | |
| D. | 纤维素属于糖类,不能被人体消化吸收,故我们不需要摄入含纤维素的食物 |
查看答案和解析>>
科目: 来源: 题型:推断题
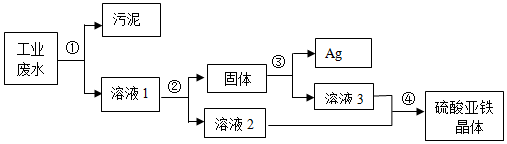
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 用燃烧法区别羊毛和合成纤维 | |
| B. | 气球充气过多爆炸 | |
| C. | 以大米、高粱、小麦等粮食为原料酿酒 | |
| D. | 铜制品在潮湿的空气中变成铜绿 |
查看答案和解析>>
科目: 来源: 题型:实验探究题
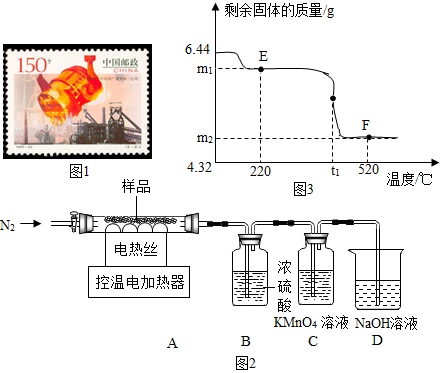
查看答案和解析>>
科目: 来源: 题型:解答题
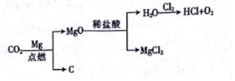
查看答案和解析>>
科目: 来源: 题型:多选题
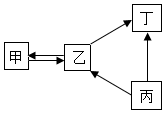 甲、乙、丙、丁均为初中化学常见物质,它们之间的部分转化关系如图所示.下列说法正确的是( )
甲、乙、丙、丁均为初中化学常见物质,它们之间的部分转化关系如图所示.下列说法正确的是( )| A. | 若甲、乙、丁都是氧化物,则丙可能是碳酸钙 | |
| B. | 若丙是碳酸钠,乙是氢氧化钠,则甲可能是硝酸钠 | |
| C. | 若甲、乙、丙、丁均含有同一种元素,且乙可用来灭火,则丙可能是氧气 | |
| D. | 甲、乙、丙、丁之间的转化不可以全部通过复分解反应实现 |
查看答案和解析>>
科目: 来源: 题型:实验探究题

查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 红磷在空气中燃烧产生大量白烟 | |
| B. | 铁丝在氧气中燃烧时,火星四射,生成四氧化三铁 | |
| C. | 木炭在氧气中燃烧发出白光,放出热量 | |
| D. | 镁和稀盐酸反应,产生无色气体,放出热量 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 蜡烛燃烧,葡萄酿酒 | B. | 汽车爆胎,石墨变为金刚石 | ||
| C. | 水果腐烂,蔗糖溶解 | D. | 玻璃破碎,鲜肉冷冻 |
查看答案和解析>>
科目: 来源: 题型:计算题
| 实验 | 1 | 2 | 3 | 5 |
| 原固体混合物质量/g | 20 | 20 | 20 | 20 |
| 加入氯化钙溶液质量/g | 20 | 40 | 60 | 80 |
| 生成的沉淀质量/g | 4 | 8 | 10 | 10 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com