
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 1.6g | B. | 2.56g | C. | 3.2g | D. | 4.8g |
查看答案和解析>>
科目: 来源: 题型:解答题
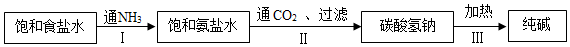
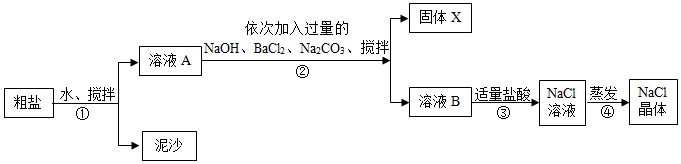
查看答案和解析>>
科目: 来源: 题型:解答题
 人类在生产和生活中广泛使用金属.请回答:
人类在生产和生活中广泛使用金属.请回答:查看答案和解析>>
科目: 来源: 题型:推断题
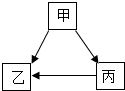 甲、乙、丙经一步反应的转化关系如图所示,其中部分反应物、生成物及反应条件已略去
甲、乙、丙经一步反应的转化关系如图所示,其中部分反应物、生成物及反应条件已略去查看答案和解析>>
科目: 来源: 题型:填空题
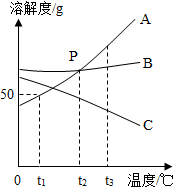 A、B、C三种固体物质的溶解度曲线如图所示,回答下列问题
A、B、C三种固体物质的溶解度曲线如图所示,回答下列问题查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
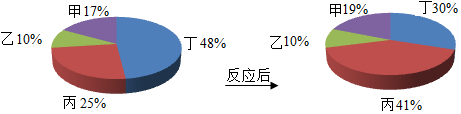 甲、乙、丙、丁四种物质在一定条件下混合反应,一段时间后,测得各物质的质量分数变化如图所示,则有关说法正确的是( )
甲、乙、丙、丁四种物质在一定条件下混合反应,一段时间后,测得各物质的质量分数变化如图所示,则有关说法正确的是( )| A. | 该反应属于分解反应 | |
| B. | 乙一定是该反应的催化剂 | |
| C. | 丁是单质 | |
| D. | 该反应生成甲和丙的质量比为19:41 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com