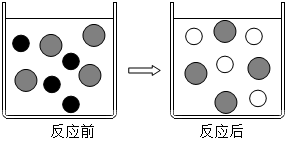
12.阅读下面科普短文(原文作者:李强、汪印等,有删改)
多孔活性炭具有较好的吸附性能,是一种优良的催化剂载体材料,广泛应用于各行各业,其生产一直以煤、竹子、木材等宝贵资源为原料.随着可持续发展理念的不断深入,越来越多的研究者尝试以清洁廉价的资源作为原料(如白酒糟),制备多孔活性炭.
白酒糟是酿酒过程的副产物,富含纤维素[(C
6H
10O
5)
n].以白酒糟为原料生产多孔活性炭的过程主要包括干燥、炭化、活化三步.炭化过程是将干燥的白酒糟在充满氮气的环境中,加热至650℃,将其中的纤维素转化为炭质原料(主要成分为单质碳).活化过程是以水蒸气或CO
2为活化剂,在一定条件下使其在炭质原料内部发生反应,生成气体,形成孔隙结构,制备多孔活性炭.以CO
2为活化剂时,发生的化学反应如下:
C+CO
2═2CO
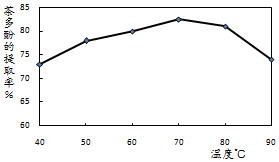
也有研究者在其他条件相同的情况下,通过实验测定所得多孔活性炭对碘的吸附值与水蒸气、CO
2用量的关系分别如图1、2所示.

尽管以白酒糟为原料,制备多孔活性炭材料的技术仍有许多问题有待于进一步探索、解决,但已有研究为富含纤维素工业残渣的利用提供了可能途径.
依据文章内容,回答下列问题.
(1)以白酒糟为原料制备多孔活性炭的优点是白酒糟是清洁廉价的资源,能够变废为宝.
(2)炭化过程中,需将干燥的白酒糟置于氮气环境中,理由是防止白酒糟与氧气反应.
(3)水蒸气与炭质原料在高温条件下发生置换反应,可生成一氧化碳.该反应的化学方程式为C+H
2O$\frac{\underline{\;高温\;}}{\;}$CO+H
2.
(4)下列说法正确的是AB(填字母序号).
A.白酒糟富含纤维素
B.多孔活性炭可用于净水
C.水蒸气用量越多,制得的多孔活性炭的吸附性能越好
(5)由图1、图2数据可知,为了达到最佳吸附效果,应选用的活化剂是水蒸气(填“水蒸气”或“CO
2”).





 Cl-、
Cl-、 H+、
H+、 Cu2+
Cu2+