
科目: 来源: 题型:推断题
 A-G表示初中化学常见的物质,其中A可用于玻璃、造纸、纺织、洗涤剂的生产,C是大理石的主要成分,各物质间相互转化关系如图所示,请回答下列问题:
A-G表示初中化学常见的物质,其中A可用于玻璃、造纸、纺织、洗涤剂的生产,C是大理石的主要成分,各物质间相互转化关系如图所示,请回答下列问题:查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 滤液中可能存在Zn2+ | B. | 滤液的颜色呈蓝色 | ||
| C. | 滤渣中一定含有Zn和Cu | D. | 滤渣中可能含Mg |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:实验探究题
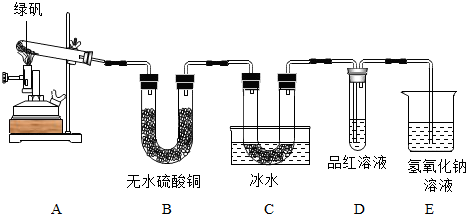
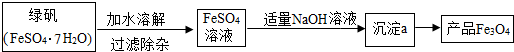
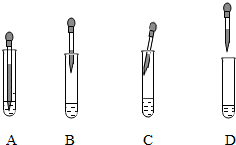
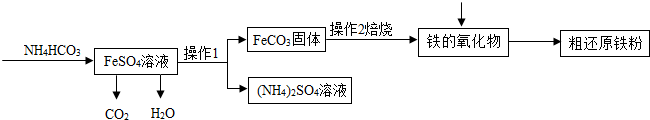
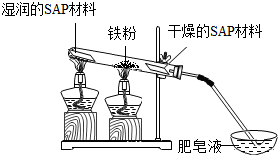
查看答案和解析>>
科目: 来源: 题型:实验探究题
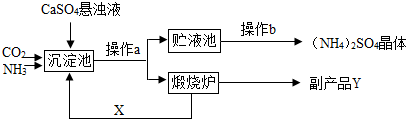
查看答案和解析>>
科目: 来源: 题型:填空题
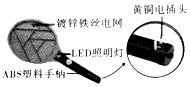 电蚊拍一般使用2.4V镍氢电池,工作时电网瞬间产生1850V直流高压电(电流小于10毫安,对人畜无害),能将蚊虫吸入电网电毙.如图是一款电蚊拍.请根据图示回答下列问题:
电蚊拍一般使用2.4V镍氢电池,工作时电网瞬间产生1850V直流高压电(电流小于10毫安,对人畜无害),能将蚊虫吸入电网电毙.如图是一款电蚊拍.请根据图示回答下列问题:查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①③⑤⑥ | B. | ①②④⑥ | C. | ②④⑤⑥ | D. | ③④⑤⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com