
科目: 来源: 题型:选择题
| A. | 臭氧与氧气的化学性质不同 | B. | 臭氧是空气质量指数的污染物之一 | ||
| C. | 汽车尾气大量排放会导致臭氧污染 | D. | 佩戴口罩能有效阻挡臭氧的吸入 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 是一种有机物 | B. | 加热会产生含硫物质 | ||
| C. | 由五种元素组成 | D. | 碳、氢原子个数之比为5:8 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:选择题
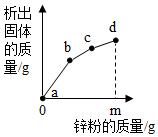 往硝酸铜、硝酸银和硝酸亚铁的混合溶液中缓慢连续加入质量为m的锌粉,溶液中析出固体的质量与参加反应的锌粉质量关系如图所示,下列说法中正确的是( )
往硝酸铜、硝酸银和硝酸亚铁的混合溶液中缓慢连续加入质量为m的锌粉,溶液中析出固体的质量与参加反应的锌粉质量关系如图所示,下列说法中正确的是( )| A. | c点对应溶液中含有的金属离子为Zn2+和Cu2+ | |
| B. | bc段(不含两端点)析出的金属是Fe | |
| C. | ab段(不含两端点)对应溶液中含有的金属离子为Zn2+、Ag+、Cu2+和Fe2+ | |
| D. | 若bc段和cd段中析出固体质量相等,参加反应的锌粉质量分别为m1和m2,则m1>m2 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O | B. | 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑ | ||
| C. | HCl+NaOH═NaCl+H2O | D. | 2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO |
查看答案和解析>>
科目: 来源: 题型:推断题
 A~F是初中化学常见的六种物质,它们之间的关系如图所示(“→”表示物质间的转化关系,“-”表示两种物质能相互反应;部分反应物、生成物及反应条件未标出).物质A可以与酸、碱、盐三类物质发生反应,D是厨房中常用的调味品,F的溶液呈黄色,反应①和②都有白色沉淀生成,请回答:
A~F是初中化学常见的六种物质,它们之间的关系如图所示(“→”表示物质间的转化关系,“-”表示两种物质能相互反应;部分反应物、生成物及反应条件未标出).物质A可以与酸、碱、盐三类物质发生反应,D是厨房中常用的调味品,F的溶液呈黄色,反应①和②都有白色沉淀生成,请回答:查看答案和解析>>
科目: 来源: 题型:推断题
 据统计,我国每年报废的手机超过1亿部,若不进行有效回收利用,会造成巨大的浪费和污染.某种手机电路板中含有以下金属:Sn、Pb、Fe、Cu、Au、Ag、Ni(镍,银白色)、Pd(钯,银白色).如图是某工厂回收其中部分金属的流程图.(假设流程图中各反应均恰好完全反应.已知:2Cu+O2+2H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$2CuSO4+2H2O)
据统计,我国每年报废的手机超过1亿部,若不进行有效回收利用,会造成巨大的浪费和污染.某种手机电路板中含有以下金属:Sn、Pb、Fe、Cu、Au、Ag、Ni(镍,银白色)、Pd(钯,银白色).如图是某工厂回收其中部分金属的流程图.(假设流程图中各反应均恰好完全反应.已知:2Cu+O2+2H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$2CuSO4+2H2O)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com