
科目: 来源: 题型:推断题
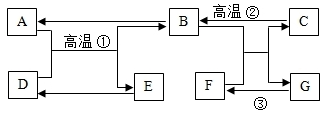
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Na2CO3、HCl、HNO3、Na2SO4 | B. | K2CO3、H2SO4、HNO3、BaCl2 | ||
| C. | HCl、AgNO3、HNO3、NaCl | D. | Na2SO4、NaOH、CuSO4、NaCl |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 滤渣是Ag、Cu、Zn | B. | 滤渣是Ag、Cu、Mg | ||
| C. | 滤液中含有Zn2+、Mg2+、NO3- | D. | 金属活动性顺序是Ag<Cu<Zn<Mg |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Ca(NO3)2、BaCl2、AgNO3 | B. | MgCl2、KOH、NaCl | ||
| C. | K2CO3、CuSO4、KCl | D. | CuSO4、Ba(OH)2、Cu(NO3)2 |
查看答案和解析>>
科目: 来源: 题型:选择题
| 物质 | a | b | c | d |
| 反应前的质量(g) | 7.4 | 4.2 | 5.0 | 3.8 |
| 反应后的质量(g) | 6.2 | x | 8.2 | 3.8 |
| A. | 物质a是生成物 | B. | x=2.2 | ||
| C. | d一定是催化剂 | D. | 反应后原子数目减少了 |
查看答案和解析>>
科目: 来源: 题型:选择题
 甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( )
甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( )| A. | t1℃时,甲、乙两物质的溶解度相等 | |
| B. | 乙物质的溶解度大于甲物质的溶解度 | |
| C. | t2℃时,乙物质的饱和溶液降温至t1℃,乙溶液变为不饱和溶液 | |
| D. | t2℃时,30g甲物质能溶解于50g水中形成80g的溶液 |
查看答案和解析>>
科目: 来源: 题型:计算题
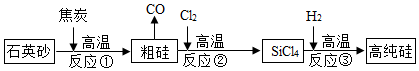
查看答案和解析>>
科目: 来源: 题型:推断题
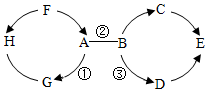 A~H为初中化学常见物质.其中A、E为氧化物且E为常见的液体,B、D为碱,H、G为单质,C为石灰石的主要成分,F为胃酸的主要成分;反应①为光合作用.它们之间的相互关系如图所示.其中“→”表示转化关系,“-”表示相互之间能发生反应(部分反应物、生成物以及反应条件省略).
A~H为初中化学常见物质.其中A、E为氧化物且E为常见的液体,B、D为碱,H、G为单质,C为石灰石的主要成分,F为胃酸的主要成分;反应①为光合作用.它们之间的相互关系如图所示.其中“→”表示转化关系,“-”表示相互之间能发生反应(部分反应物、生成物以及反应条件省略).查看答案和解析>>
科目: 来源: 题型:解答题
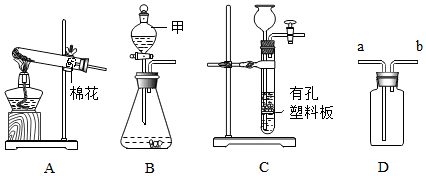
查看答案和解析>>
科目: 来源: 题型:多选题
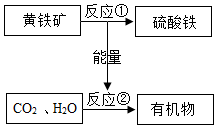 “细菌冶金”的原理是利用氧化铁硫杆菌促使 黄铁矿(主要成分FeS2)氧化成硫酸铁和硫酸,并能为CO2和H2O合成有机物提供能量.流程如图,下列说法错误的是( )
“细菌冶金”的原理是利用氧化铁硫杆菌促使 黄铁矿(主要成分FeS2)氧化成硫酸铁和硫酸,并能为CO2和H2O合成有机物提供能量.流程如图,下列说法错误的是( )| A. | 反应①化学方程式:4FeS2+15O2+2X=2Fe2(SO4)3+2H2SO4,X为H2O2 | |
| B. | 整个流程提高了能量的利用率 | |
| C. | 图中有机物一定不含氧元素 | |
| D. | 氧化铁硫杆菌在反应①中起催化作用 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com