
科目: 来源: 题型:选择题
| A. | 活性炭可以将硬水软化 | |
| B. | 湿衣服在阳光下比阴凉处干得快,原因是水分子受热后运动速率加快 | |
| C. | 可用打火机检查天然气是否泄露 | |
| D. | 过氧化氢分子能分解成水分子和氧分子,说明分子是化学变化中的最小微粒 |
查看答案和解析>>
科目: 来源: 题型:实验探究题
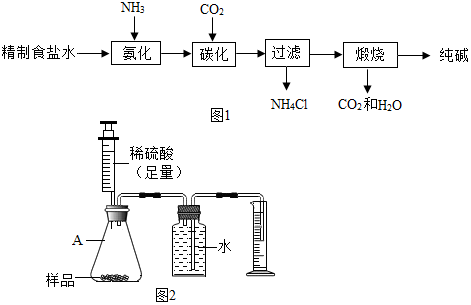
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 该反应不符合复分解反应发生的条件 | |
| B. | 该反应中四种物质都是盐 | |
| C. | 反应后可用过滤的方法分离出NaHCO3 | |
| D. | 反应后的溶液中还能继续溶解NaCl |
查看答案和解析>>
科目: 来源: 题型:计算题
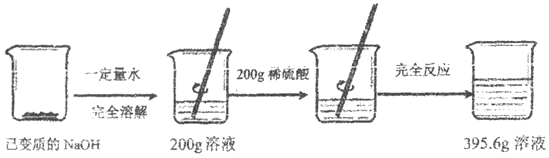
查看答案和解析>>
科目: 来源: 题型:实验探究题
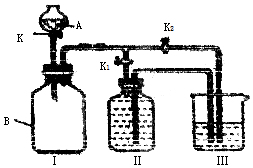
查看答案和解析>>
科目: 来源: 题型:实验探究题
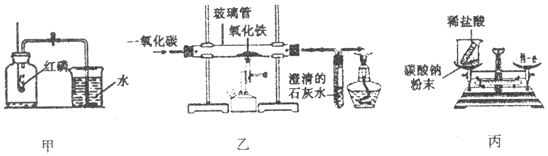
查看答案和解析>>
科目: 来源: 题型:推断题
查看答案和解析>>
科目: 来源: 题型:选择题
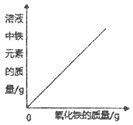 | 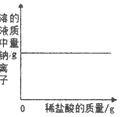 | 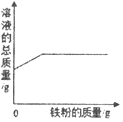 |  |
| A.向一定量的稀盐酸中加入氧化铁 | B.向一定量的氢氧化钠溶液中滴加稀盐酸 | C.向一定量的硫酸铜溶液中加入铁粉 | D.向一定量的氢氧化钠和氢氧化钙的混合溶液中通入二氧化碳 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com