
科目: 来源: 题型:实验探究题
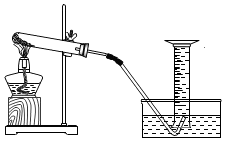 在用氯酸钾和二氧化锰的混合物制取氧气实验后,为了进一步探究二氧化锰的用量对氯酸钾分解速度的影响,小明用如图装置,以及实验室提供的实验所需药品和器材进行实验,老师对实验的建议:①每组实验氯酸钾用量可取4克,二氧化锰质量不宜超过2克.②实验设计4组.
在用氯酸钾和二氧化锰的混合物制取氧气实验后,为了进一步探究二氧化锰的用量对氯酸钾分解速度的影响,小明用如图装置,以及实验室提供的实验所需药品和器材进行实验,老师对实验的建议:①每组实验氯酸钾用量可取4克,二氧化锰质量不宜超过2克.②实验设计4组.查看答案和解析>>
科目: 来源: 题型:解答题
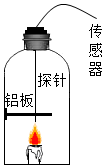 蜡烛(主要含C、H、O元素)在密闭容器中熄灭的原因是什么?燃烧的产物是什么?小敏认为蜡烛熄灭的原因是燃烧消耗完了容器内的氧气,并对燃烧产物提出猜想:
蜡烛(主要含C、H、O元素)在密闭容器中熄灭的原因是什么?燃烧的产物是什么?小敏认为蜡烛熄灭的原因是燃烧消耗完了容器内的氧气,并对燃烧产物提出猜想:| 相对湿度 | 氧气含量 | 二氧化碳含量 | 一氧化碳含量 | |
| 蜡烛点燃前 | 48.4% | 18.7% | 0.058% | 0 |
| 蜡烛熄灭后 | 71.6% | 15.6% | 3.643% | 0.018% |
查看答案和解析>>
科目: 来源: 题型:实验探究题
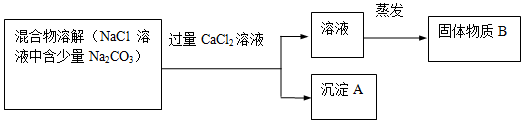
查看答案和解析>>
科目: 来源: 题型:实验探究题
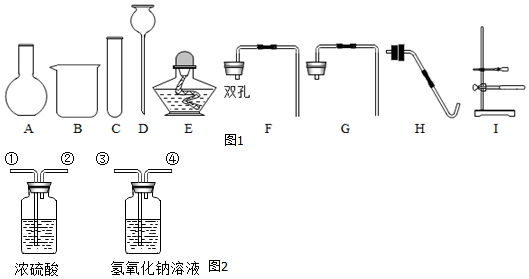
查看答案和解析>>
科目: 来源: 题型:填空题
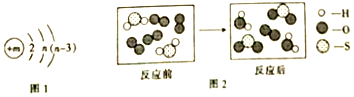
查看答案和解析>>
科目: 来源: 题型:选择题
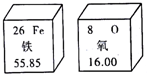
| A. | 氧原子的核外电子数为8 | |
| B. | 铁元素和氧元素都属于非金属元素 | |
| C. | 铁的相对原子质量是55.85g | |
| D. | 铁元素与氧元素只能组成一种化合物 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 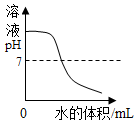 向一定量4%的NaOH溶液中不断加水 | |
| B. | 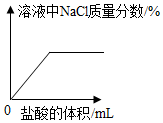 向一定量的NaOH溶液中逐滴加入稀盐酸至过量 | |
| C. | 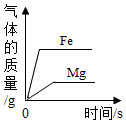 常温下,将等质量的铁和镁分别同时投入足量.等质量分数的稀盐酸中 | |
| D. | 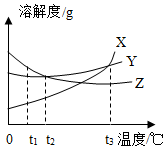 将t3℃时X、Y、Z三种物质的饱和溶液降温到t1℃,所得溶液中溶质的质量分数由大到小的顺序为Y>Z>X |
查看答案和解析>>
科目: 来源: 题型:解答题
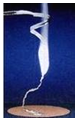 化学兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验(如右图),同学们观察到镁条在空气中剧烈燃烧,发出耀眼的强光,产生的大量白烟弥漫到空气中,最后在石棉网上得到一些白色固体.
化学兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验(如右图),同学们观察到镁条在空气中剧烈燃烧,发出耀眼的强光,产生的大量白烟弥漫到空气中,最后在石棉网上得到一些白色固体.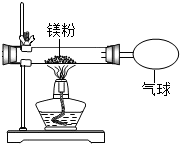
| 实验操作 | 实验现象及结论 |
| 取少量黄色固体于试管中,加入适量的水,并将湿润的红色石蕊试纸放在试管口 | 试管中有气体产生,湿润的红色石蕊试纸变蓝.得出结论:黄色固体是Mg3N2 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 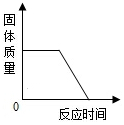 用一氧化碳气体还原一定质量的氧化铁粉末 | |
| B. | 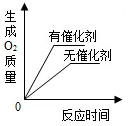 用两份等质量、等浓度的过氧化氢溶液分别制取氧气 | |
| C. | 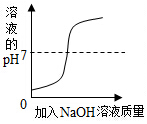 向一定体积的稀盐酸中逐滴加入足量的氢氧化钠溶液 | |
| D. | 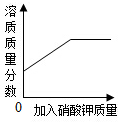 某温度下,向一定量饱和硝酸钾溶液中加入硝酸钾晶体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com