
科目: 来源: 题型:选择题
| A. | R中含有硫、氧元素 | |
| B. | R的相对分子质量为76 | |
| C. | R燃烧后的两种生成物都会污染大气 | |
| D. | 参加反应的R的质量为14g |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. |  | B. |  | C. |  | D. |  |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:计算题
| 实验次数 | 1 | 2 | 3 | 4 | 5 |
| 加入NaOH溶液质量/g | 40 | 40 | 40 | 40 | 40 |
| 共生成沉淀的质量/g | 2.9 | 5.8 | m | 11.6 | 11.6 |
查看答案和解析>>
科目: 来源: 题型:推断题
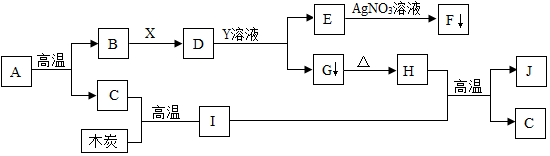
查看答案和解析>>
科目: 来源: 题型:选择题
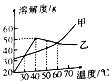
| A. | 30℃时,甲、乙的溶解度相同 | |
| B. | 将甲的溶液降温,一定有晶体析出 | |
| C. | 40℃时,乙饱和溶液比甲饱和溶液溶质质量分数大 | |
| D. | 甲、乙都属于易溶物质 |
查看答案和解析>>
科目: 来源: 题型:选择题
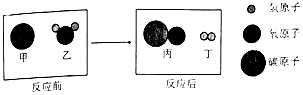
| A. | 反应前后原子的种类、数目都不变 | B. | 该反应是置换反应 | ||
| C. | 反应中甲、乙两物质的质量比为1:1 | D. | 乙、丙两种物质都是氧化物 |
查看答案和解析>>
科目: 来源: 题型:实验探究题
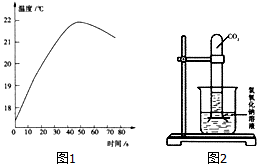 小组同学在学完中和反应知识后思考,除了通过酚酞变色说明氧氧化钠与稀盐酸能发生反应,还有什么方法能说明两者发生了反应?同学们讨论后进行以下实验探究.
小组同学在学完中和反应知识后思考,除了通过酚酞变色说明氧氧化钠与稀盐酸能发生反应,还有什么方法能说明两者发生了反应?同学们讨论后进行以下实验探究.查看答案和解析>>
科目: 来源: 题型:实验探究题
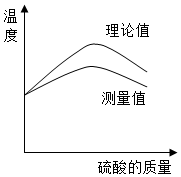 实验小组同学欲利用氢氧化钠溶液与硫酸探究中和反应中的热量变化.请你参与探究实验.
实验小组同学欲利用氢氧化钠溶液与硫酸探究中和反应中的热量变化.请你参与探究实验.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com