
科目: 来源: 题型:选择题
| A. | 由C、H、N、P、O五个元素组成 | B. | 碳、氧元素的质量之比是3:2 | ||
| C. | 相对分子质量为410 | D. | 一个分子中含有58个原子 |
查看答案和解析>>
科目: 来源: 题型:计算题
 向盛有22.3gNa2CO3和NaCl固体混合物的烧杯中加入216.1g稀盐酸恰好反应,反应过程用精密仪器测得烧杯连同药品的质量(m)与反应时间(t)的关系如下图所示:烧杯连同药品的起始质量为300g.
向盛有22.3gNa2CO3和NaCl固体混合物的烧杯中加入216.1g稀盐酸恰好反应,反应过程用精密仪器测得烧杯连同药品的质量(m)与反应时间(t)的关系如下图所示:烧杯连同药品的起始质量为300g.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:计算题
查看答案和解析>>
科目: 来源: 题型:填空题
 某溶液由NaOH、HCl、H2SO4和CuCl2中的一种或几种组成,向该溶液滴加Ba(OH)2溶液,产生沉淀的质量与加入Ba(OH)2溶液体积的关系如图所示.
某溶液由NaOH、HCl、H2SO4和CuCl2中的一种或几种组成,向该溶液滴加Ba(OH)2溶液,产生沉淀的质量与加入Ba(OH)2溶液体积的关系如图所示.查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 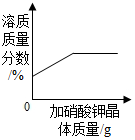 某温度下,向一定量的硝酸钾饱和溶液中不断加入硝酸钾晶体 | |
| B. | 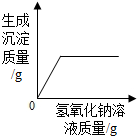 向稀盐酸和氯化铜的混合溶液中加入过量的氢氧化钠溶液 | |
| C. | 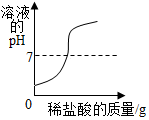 向氢氧化钠溶液中滴加过量的稀盐酸 | |
| D. | 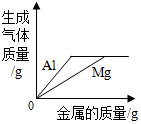 向盛有等质量、等溶质质量分数的稀硫酸的两支试管中,分别加入过量的金属镁和铝 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 甲车间的污水中不可能含有Na+和Cl- | |
| B. | 乙车间的污水中可能含有Ag+和NO3- | |
| C. | 甲车间的污水中可能含有Ba2+和OH- | |
| D. | 乙车间的污水中不可能含有Fe3+和SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com