
科目: 来源: 题型:实验探究题
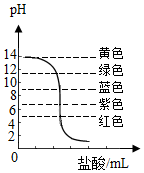 老师在第十单元课题2“酸和碱的中和反应”课堂中演示了酸碱中和滴定实验,但对实验进行了改进,并对两个问题进行了讨论.
老师在第十单元课题2“酸和碱的中和反应”课堂中演示了酸碱中和滴定实验,但对实验进行了改进,并对两个问题进行了讨论.查看答案和解析>>
科目: 来源: 题型:实验探究题
查看答案和解析>>
科目: 来源: 题型:实验探究题
查看答案和解析>>
科目: 来源: 题型:实验探究题
查看答案和解析>>
科目: 来源: 题型:解答题
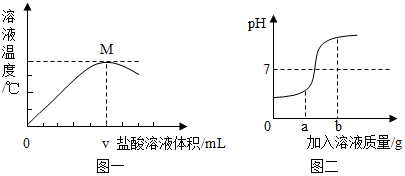
查看答案和解析>>
科目: 来源: 题型:实验探究题
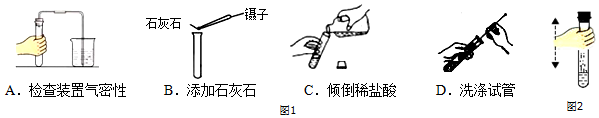
查看答案和解析>>
科目: 来源: 题型:实验探究题
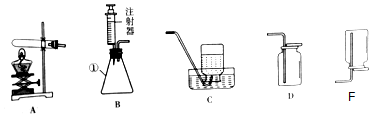
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
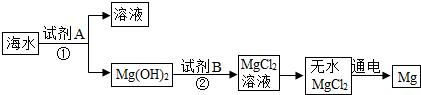
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 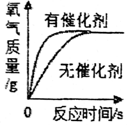 用等质量、等浓度的过氧化氢溶液在有无催化剂条件下制氧气 | |
| B. | 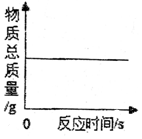 一定质量的红磷在密闭容器中燃烧 | |
| C. |  向一定质量的饱和石灰水中加入氧化钙 | |
| D. | 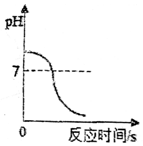 向一定量稀盐酸溶液中逐滴加入氢氧化钠溶液至过量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com