
科目: 来源: 题型:实验探究题
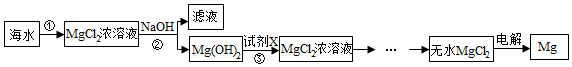
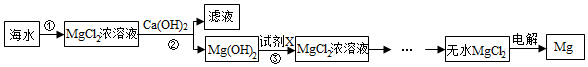
| 试剂 | NaOH | Ca(OH)2 |
| 价格(元/t) | 3200 | 1200 |
查看答案和解析>>
科目: 来源: 题型:实验探究题
| 探究内容 | 现象 |
| 实验1:取一定量的肥料放入水中,振荡 | 样品完全溶解 |
| 实验2:取实验1中的部分溶液,滴入石蕊试剂, | 溶液呈红色 |
| 实验3:另取实验1中的部分溶液,滴加氯化钡试剂与稀盐酸, | 有白色沉淀生成 |
查看答案和解析>>
科目: 来源: 题型:选择题
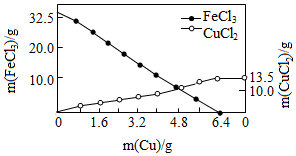 FeCl3溶液常用于蚀刻印刷电路,反应原理为aFeCl3+bCu═cCuCl2+dX.向含溶质32.5g的FeCl3溶液中慢慢加入一定量的Cu粉,反应过程中FeCl3、CuCl2的质量随Cu粉质量变化如图.下列说法不正确的是( )
FeCl3溶液常用于蚀刻印刷电路,反应原理为aFeCl3+bCu═cCuCl2+dX.向含溶质32.5g的FeCl3溶液中慢慢加入一定量的Cu粉,反应过程中FeCl3、CuCl2的质量随Cu粉质量变化如图.下列说法不正确的是( )| A. | X为FeCl2 | B. | 化学计量数c=1 | ||
| C. | 方程式中a和b的比为1:2 | D. | 完全反应后,生成X的质量为25.4g |
查看答案和解析>>
科目: 来源: 题型:实验探究题
查看答案和解析>>
科目: 来源: 题型:选择题
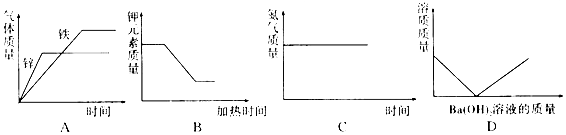
| A. | 形状和质量相同的铁和锌分别加入到足量的同一种稀硫酸中 | |
| B. | 加热高锰酸钾 | |
| C. | 足量红磷在装有空气的密闭容器中燃烧 | |
| D. | 稀硫酸中滴入氢氧化钡溶液 |
查看答案和解析>>
科目: 来源: 题型:实验探究题
查看答案和解析>>
科目: 来源: 题型:实验探究题
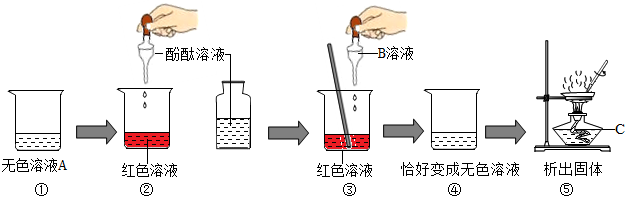
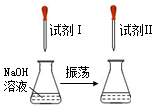 小刚同学选择了稀盐酸、氢氧化钠溶液、酚酞溶液三种试剂,按如图所示进行酸碱中和反应的实验.请回答:
小刚同学选择了稀盐酸、氢氧化钠溶液、酚酞溶液三种试剂,按如图所示进行酸碱中和反应的实验.请回答:查看答案和解析>>
科目: 来源: 题型:实验探究题
查看答案和解析>>
科目: 来源: 题型:实验探究题
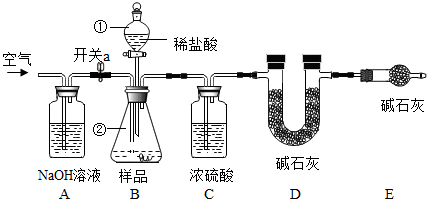
查看答案和解析>>
科目: 来源: 题型:解答题
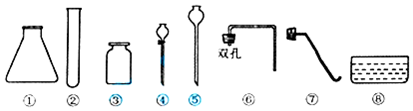
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com