
科目: 来源: 题型:实验探究题
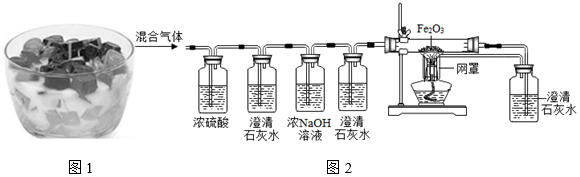
| 步骤 | 现象 | 分析 |
| (1)点燃“果冻蜡烛”,并在火焰上方罩一个干燥的小烧杯 | 烧杯内壁有无色小液滴生成 | “果冻蜡烛”在燃烧后的产物有水 |
| (2)迅速倒转小烧杯,向其中加入适量澄清石灰水,振荡. | 澄清石灰水变浑浊 | “果冻蜡烛”在燃烧后的产物有二氧化碳 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:实验探究题
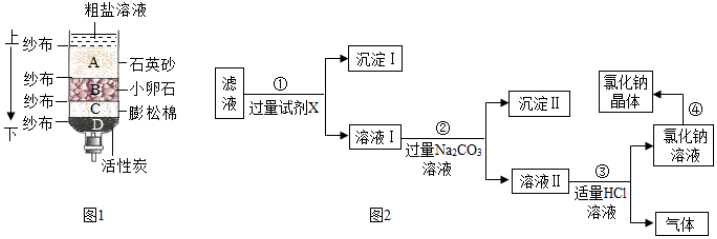
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:推断题
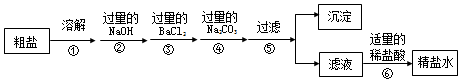
查看答案和解析>>
科目: 来源: 题型:填空题
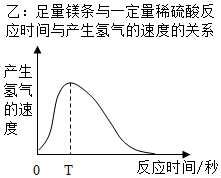 表格和图象能直观反应物质的变化规律.请根据下列表格和图象,回答有关问题:
表格和图象能直观反应物质的变化规律.请根据下列表格和图象,回答有关问题:| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 |
| NH4Cl溶解度/g | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
| NaCl溶解度/g | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
查看答案和解析>>
科目: 来源: 题型:实验探究题
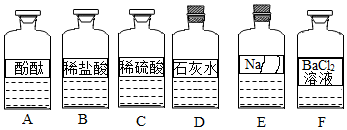
| 实验方案 | 实验一 | 实验二 | 实验三 |
| 实验操作 | 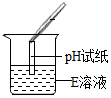 | 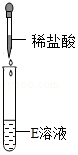 |  |
| 实验现象 | 试纸变色,对照比色卡,pH>7 | 有无色无味气体产生 | 出现白色沉淀 |
| 实验结论 | 猜想Ⅱ正确 | ||
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题

查看答案和解析>>
科目: 来源: 题型:实验探究题
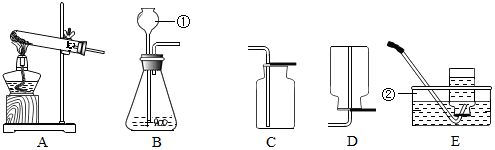
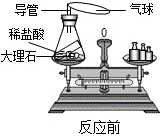 小明设计了一个实验来探究质量守恒定律.如图所示,反应前天平平衡,他取下此装置(装置气密性良好)将其倾斜,使稀盐酸(HCl)和大理石(主要成分是碳酸钙)接触,生成氯化钙、二氧化碳气体和水,待充分反应后,气球膨胀,再将装置放回天平左盘,此时他发现天平的指针向右偏转了.请回答下列问题:
小明设计了一个实验来探究质量守恒定律.如图所示,反应前天平平衡,他取下此装置(装置气密性良好)将其倾斜,使稀盐酸(HCl)和大理石(主要成分是碳酸钙)接触,生成氯化钙、二氧化碳气体和水,待充分反应后,气球膨胀,再将装置放回天平左盘,此时他发现天平的指针向右偏转了.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com