
科目: 来源: 题型:实验探究题
查看答案和解析>>
科目: 来源: 题型:实验探究题
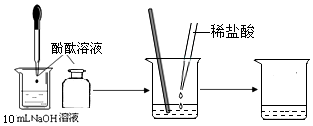
 化学兴趣小组同学进行中和反应实验时,将4mL2%的稀硫酸逐滴滴加到2mL2%的氢氧化钠溶液中,测得溶液的pH变化曲线如图所示.
化学兴趣小组同学进行中和反应实验时,将4mL2%的稀硫酸逐滴滴加到2mL2%的氢氧化钠溶液中,测得溶液的pH变化曲线如图所示.| 实验操作 | 实验现象 | 实验分析 |
| 取适量a处溶液于试管中,加入镁条 | 无气泡产生 | 溶液中几乎不含H+(填离子符号) |
| 取适量b处溶液于试管中,加入紫色石蕊溶液 | 石蕊溶液不变色 | 溶液中几乎不含H+和OH- |
| 取适量c处溶液于试管中,加入硫酸铜溶液 | 无沉淀产生 | 溶液中几乎不含OH- |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:实验探究题

查看答案和解析>>
科目: 来源: 题型:实验探究题
| 实验步骤 | 实 验 现 象 | 结 论 |
| 分别把这两种金属放入稀盐酸 溶液中,观察. | 金属Y表面无明显变化;金属X的表面有大量气泡冒出.将燃着的木条放在金属X的试管口,气体燃烧. | 金属活动性顺序:X>Y |
查看答案和解析>>
科目: 来源: 题型:解答题
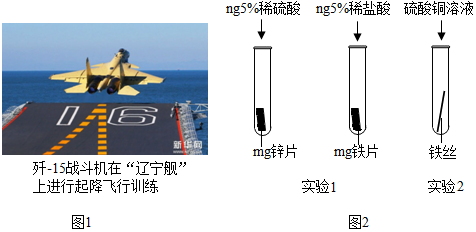
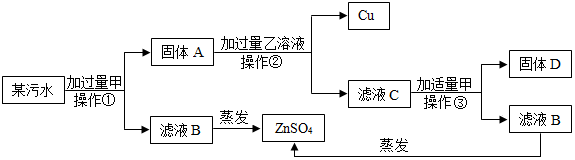
 为探究锌、铁、铜三种金属的活动性顺序,某学习小组做了如图甲所示实验,通过试管①内的无明显变化现象,试管②内的析出红色固体,溶液由蓝色变成浅绿色现象可推测出三种金属的活动性顺序,写出涉及的化学方程式Fe+CuCl2=FeCl2+Cu.实验室结束后,将试管①、试管②内的物质全部倒入同一烧杯中,充分反应后发现烧杯中的红色固体物质明显增多(如图乙所示),则甲图试管②中反应后固体一定含有铜,一定不含铁.
为探究锌、铁、铜三种金属的活动性顺序,某学习小组做了如图甲所示实验,通过试管①内的无明显变化现象,试管②内的析出红色固体,溶液由蓝色变成浅绿色现象可推测出三种金属的活动性顺序,写出涉及的化学方程式Fe+CuCl2=FeCl2+Cu.实验室结束后,将试管①、试管②内的物质全部倒入同一烧杯中,充分反应后发现烧杯中的红色固体物质明显增多(如图乙所示),则甲图试管②中反应后固体一定含有铜,一定不含铁.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 紫色石蕊 | B. | 无色酚酞 | C. | Na2CO3 | D. | AgNO3 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ②⑤ | B. | ③⑤ | C. | ①②⑤ | D. | ②④⑥ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 塑料属于有机合成高分子材料 | |
| B. | 玻璃属于有机高分子合成材料 | |
| C. | 开发使用可降解塑料能有效解决“白色污染”问题 | |
| D. | 合成材料的大量使用给人类带来了严重污染 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com