
科目: 来源: 题型:计算题
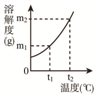 如图为固体A的溶解度曲线图.
如图为固体A的溶解度曲线图.查看答案和解析>>
科目: 来源: 题型:实验探究题

| 试管中硝酸钾的总量/g | 5 | 6.5 | 8 | 10 | 12.5 |
| 开始析出晶体时的温度t/℃ | 32.8 | 39.6 | 45.8 | 54.7 | 64.9 |
| 溶解度/g | 50 | 65 | 80 | 125 |

查看答案和解析>>
科目: 来源: 题型:计算题
查看答案和解析>>
科目: 来源: 题型:填空题
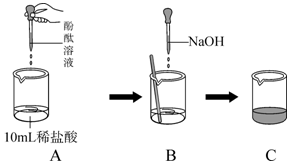
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 偏小 | B. | 偏大 | ||
| C. | 无影响 | D. | 以上选项均有可能 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | H2CO3═CO2↑+H2O (分解反应) | B. | CuO+H2SO4═CuSO4+H2O (中和反应) | ||
| C. | 2Na+2H2O═2NaOH+H2↑ (置换反应) | D. | CaO+H2O═Ca(OH)2 (化合反应) |
查看答案和解析>>
科目: 来源: 题型:实验探究题
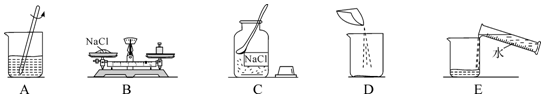
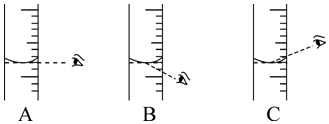
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com