
科目: 来源: 题型:选择题
 松花江滨州铁路桥俗称“老江桥”,始建于1901年,是松花江上最早的铁路大桥,这是中东铁路桥的第一座跨江桥梁,是横穿欧亚大陆的中东铁路的松花江铁路桥.随着新建铁路桥竣工脚步的临近,这座老桥将完成它的历史使命.下列有关叙述错误的是( )
松花江滨州铁路桥俗称“老江桥”,始建于1901年,是松花江上最早的铁路大桥,这是中东铁路桥的第一座跨江桥梁,是横穿欧亚大陆的中东铁路的松花江铁路桥.随着新建铁路桥竣工脚步的临近,这座老桥将完成它的历史使命.下列有关叙述错误的是( )| A. | 松花江铁路桥是沙俄通过《中俄密约》攫取了铁路修筑权,是沙俄侵占我东北领土的历史见证 | |
| B. | 桥墩为石膏白灰浆砌石,花岗岩石镶面,石灰浆的主要成分为氧化钙 | |
| C. | 老江桥为钢筋架墩结构,钢筋的成分是铁的合金 | |
| D. | 桥体上加装的灯饰外壳采用的材料为合成材料 |
查看答案和解析>>
科目: 来源: 题型:填空题
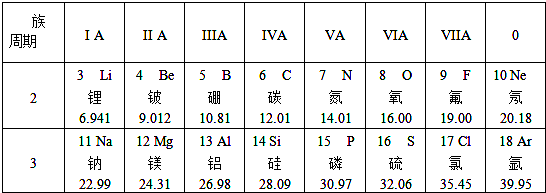
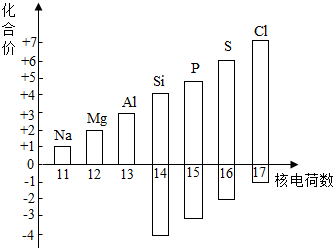 了解物质的组成和结构,有助于认识物质的性质.
了解物质的组成和结构,有助于认识物质的性质.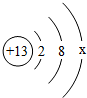 ,则最外层电子数x=3;若最外层电子失去,达到相对稳定结构,该带电粒子的符号为Al3+.
,则最外层电子数x=3;若最外层电子失去,达到相对稳定结构,该带电粒子的符号为Al3+.查看答案和解析>>
科目: 来源: 题型:填空题
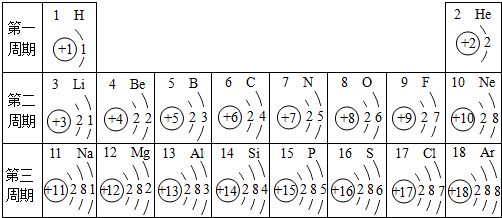
查看答案和解析>>
科目: 来源: 题型:填空题

 化学反应中该原子比较容易得到(填“得到”或“失去”)电子变成S2-(填离子符号)
化学反应中该原子比较容易得到(填“得到”或“失去”)电子变成S2-(填离子符号)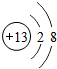 表示的是Al3+(填离子符号);
表示的是Al3+(填离子符号);查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题
 广西矿产资源丰富,铟的生产规模居世界同类企业首位.图1中是元素周期表中铟元素的信息,图2是铟原子的结构示意图,回答下列问题.
广西矿产资源丰富,铟的生产规模居世界同类企业首位.图1中是元素周期表中铟元素的信息,图2是铟原子的结构示意图,回答下列问题. ,该元素与铟元素在元素周期表中处于同一个族(填“周期”或“族”)
,该元素与铟元素在元素周期表中处于同一个族(填“周期”或“族”)查看答案和解析>>
科目: 来源: 题型:解答题
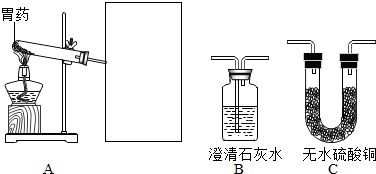
| 实验过程 | 实验现象 | 实验结论 |
| 乙同学选用B、C装置,按A→B→C顺序连接,点燃酒精灯加热 | B中澄清石灰水变浑浊, C中无水硫酸铜变为蓝色. | 该胃药中含有MgCO3、Al(OH)3 |
| 丙同学也选用B、C装置,按A→C→B顺序连接,点燃酒精灯加热 | C中无明显现象,B中澄清石灰水变浑浊. | 该胃药中不含有Al(OH)3或氢氧化铝 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
| 实验步骤 | 实验现象 | 实验结论 |
| (1)取适量电石加水反应,收集生成的气体,验纯后点燃. | 气体燃烧,产生黄色火焰并伴有浓烈黑烟. | 电石与水反应产生的气体是乙炔(或C2H2) |
| (2)取适量反应后生成的固体于试管中,滴加过量稀盐酸. | 固体溶解,无气泡放出. | 电石与水反应产生的固体不是碳酸钙 |
| (3)取适量反应后生成的固体于试管中加水,向上层清液中滴加2~3滴酚酞. | 溶液变红 | 电石与水反应产生的固体是氢氧化钙 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com