
科目: 来源: 题型:选择题
| A. | 红磷在空气中燃烧,产生大量白烟 | B. | 木炭在氧气中燃烧,发出白光 | ||
| C. | 细铁丝在氧气中燃烧,火星四射 | D. | 硫在氧气中燃烧,火焰呈淡蓝色 |
查看答案和解析>>
科目: 来源: 题型:选择题
| 选项 | 操作或现象 | 分子的特性 |
| ① | 25m3的石油气在加压装入容积为0.024m3的钢瓶中 | 分子间有间隔 |
| ② | 经过加油站常闻到汽油的气味 | 分子是运动的 |
| ③ | 100mL氧气和100mL氮气混合在一起,体积小于200mL | 分子的质量非常小 |
| ④ | 加热氧化汞可得到金属汞和氧气 | 分子是可以再分的 |
| A. | ① | B. | ② | C. | ③ | D. | ④ |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
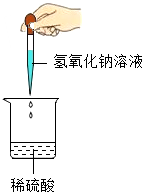 某学习小组的同学在做氢氧化钠溶液与稀硫酸的中和反应实验时(如下图所示),忽然发现没有加入指示剂.于是将实验改为探究烧杯内溶液中溶质的成分.
某学习小组的同学在做氢氧化钠溶液与稀硫酸的中和反应实验时(如下图所示),忽然发现没有加入指示剂.于是将实验改为探究烧杯内溶液中溶质的成分.| 实验步骤 | 实验现象 | 实验结论与解释 |
| 取少量烧杯中溶液于试管中,加入锌(填试剂名称) | 有气泡产生 | 溶质还有硫酸反应的化学方程式为Zn+H2SO4=ZnSO4+H2↑ |
查看答案和解析>>
科目: 来源: 题型:解答题

| 实验编号 | 选用金属 (均取2g) | 盐酸质量分数 (均取50mL) | 每分钟产生氢气的体积/mL | |||||
| 1分钟 | 1~2分钟 | 2~3 分钟 | 3~4分钟 | 4~5分钟 | 前5分钟共收集气体 | |||
| 1 | 锌片 | 15% | 2.9 | 16.9 | 11.9 | 9.2 | 7.6 | 48.5 |
| 2 | 锌片 | 5% | 1.6 | 8.4 | 5.9 | 4.8 | 3.7 | 24.4 |
查看答案和解析>>
科目: 来源: 题型:填空题
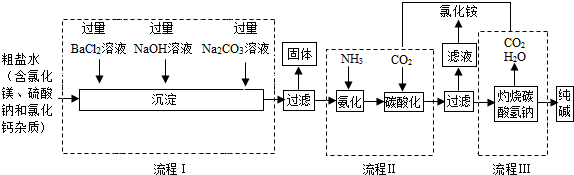
查看答案和解析>>
科目: 来源: 题型:填空题
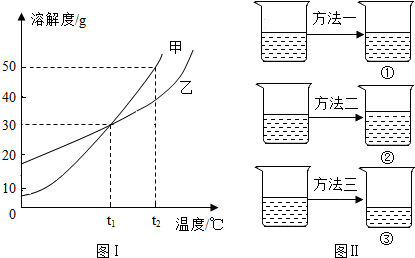
查看答案和解析>>
科目: 来源: 题型:填空题

查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| 选项 | 分类 | 举例 |
| A | 常见合金 | 生铁、不锈钢、青铜 |
| B | 常见酸 | 盐酸、硫酸、醋酸 |
| C | 常见碱 | 熟石灰 纯碱 氨水 |
| D | 常见干燥剂 | 浓硫酸、生石灰、烧碱 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com