
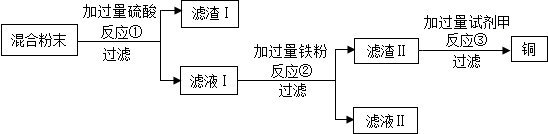
科目: 来源: 题型:解答题
查看答案和解析>>
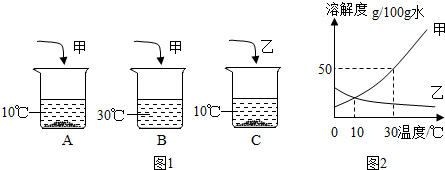
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题
| 添加剂名称 | 主要化学性质及在体内变化 |
| 碳酸氢钠 | 无毒、弱碱性,易与胃酸反应,加热分解成碳酸钠、水和二氧化碳 |
| 铁 (还原性铁粉) | 比较活泼的金属,能与胃酸反应 |
| 食盐 | 易溶、中性,与硝酸银溶液反应生成白色沉淀 |
| 亚硝酸钠 | 易溶、水溶液显碱性,跟硝酸银反应生成浅黄色沉淀 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 12.5g | B. | 22.5g | C. | 25g | D. | 20.83g |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 氯化钾 | B. | 硝酸钾 | C. | 氯化钠 | D. | 硝酸钠 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 生成气体的质量可能是11克或33克 | |
| B. | 滤渣中的红色物质可能是32克或96克 | |
| C. | 参与反应的氧化铜质量可能是40克或120克 | |
| D. | 稀硫酸的溶质质量可能是38.4克或115.2克 |
查看答案和解析>>
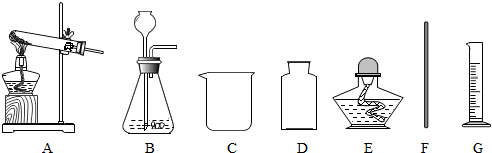
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
 陈程同学经常采用构建知识网络的方法学习化学.如他将某些物质相互关系构建为如图所示的知识网络图(“→”表示这种物质转化为另一种物质).回答下列问题:
陈程同学经常采用构建知识网络的方法学习化学.如他将某些物质相互关系构建为如图所示的知识网络图(“→”表示这种物质转化为另一种物质).回答下列问题:查看答案和解析>>
科目: 来源: 题型:解答题
| 实验步骤 | 现象与结论 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com