
科目: 来源: 题型:选择题
| A. | 用熟石灰和硫酸铜配制波尔多液 | |
| B. | 服用含Mg(OH)2的药物治疗胃酸过多 | |
| C. | 施用熟石灰改良酸性土壤 | |
| D. | 用氨水与工厂排放的含硫酸的废水反应制氮肥 |
查看答案和解析>>
科目: 来源: 题型:解答题
 如图是a、b、c三种物质的溶解度曲线a与c的溶解度曲线相交于P点.据图回答:
如图是a、b、c三种物质的溶解度曲线a与c的溶解度曲线相交于P点.据图回答:查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题

| 反应前 | 反应后 |
| E的质量为100.0g | E的质量为102.25g |
| F的质量为50.0g | F的质量为51.1g |
查看答案和解析>>
科目: 来源: 题型:选择题
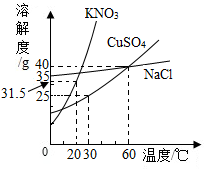 如图是几种盐的溶解度曲线,下列说法正确的是( )
如图是几种盐的溶解度曲线,下列说法正确的是( )| A. | 40℃时,将35g食盐溶于100g水中,降温至0℃可析出NaCl晶体 | |
| B. | 20℃时,KNO3饱和溶液的质量分数 是31.5% | |
| C. | 60℃时,200g水中溶解80g硫酸铜达饱和,当降温至30℃可析出30g硫酸铜晶体 | |
| D. | 30℃时,将35gNaCl和35gKNO3同时溶于100g水中,蒸发时先析出NaCl |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 13.04% | B. | 18.25% | C. | 17.05% | D. | 无法计算 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 混合后溶液的质量为200g | B. | 混合溶液的pH=7 | ||
| C. | 混合后溶液中只有一种溶质 | D. | 所得溶液中加入锌粒可产生气泡 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ① | B. | ①④ | C. | ②③④ | D. | ①②③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com