
科目: 来源: 题型:解答题
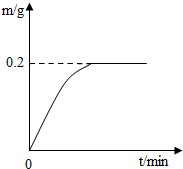 日常生活中接触的金属材料,大多属于合金.其中黄铜是以锌作主要添加元素的铜合金.已知组成某弹壳的黄铜中只含有锌和铜,现将22g该弹壳碾成粉末后放入盛有足量的稀硫酸烧杯中,测得反应过程中生成的氢气的质量(单位为g)与反应时间(单位为min)的关系如图所示.试计算:
日常生活中接触的金属材料,大多属于合金.其中黄铜是以锌作主要添加元素的铜合金.已知组成某弹壳的黄铜中只含有锌和铜,现将22g该弹壳碾成粉末后放入盛有足量的稀硫酸烧杯中,测得反应过程中生成的氢气的质量(单位为g)与反应时间(单位为min)的关系如图所示.试计算:查看答案和解析>>
科目: 来源: 题型:解答题
| 氯化钾 | 氯化钙 | 氯化钠 | 氯化镁 | 氯化铝 | 氯化锌 | 氯化亚铁 | 氯化铜 |
| KCl | CaCl2 | NaCl | MgCl2 | AlCl3 | ZnCl2 | FeCl2 | CuCl2 |

| NaCl溶液 | CuSO4溶液 | K2CO3溶液 | |
| 甲同学 | 7 | 4 | 10 |
| 乙同学 | 7 | 5 | 9 |
查看答案和解析>>
科目: 来源: 题型:解答题
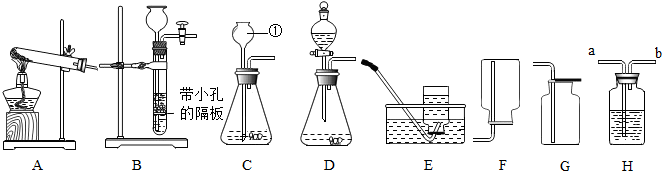
 某教师设计的创新实验装置图如图,请完成下列探究:
某教师设计的创新实验装置图如图,请完成下列探究:查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
 2014年6月10日是“全国低碳日”,“节能减排,低碳生活”的主题旨在倡导节约能源和利用清洁能源,减少温室气体二氧化碳的排放.下列做法符合“主题是C
2014年6月10日是“全国低碳日”,“节能减排,低碳生活”的主题旨在倡导节约能源和利用清洁能源,减少温室气体二氧化碳的排放.下列做法符合“主题是C查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 酸碱发生中和反应生成盐和水,所以生成盐和水的反应一定是中和反应 | |
| B. | 酸溶液中都含有氢离子,所以含有氢元素的物质一定是酸 | |
| C. | 有机物都含有碳元素,所以含有碳元素的化合物一定是有机物 | |
| D. | 化合物是由不同元素组成的纯净物,所以只含一种元素的物质一定不是化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com