
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:解答题
| 商品 |  |  |  |
| 成分 | 碳酸钠 | 碳酸氢钠 | 碳酸氢钠、有机酸 |
| 性质 | 碳酸钠 | 碳酸氢钠 |
| 溶解性 | 20℃时溶解度21.6g,溶解时放热 | 20℃时溶解度9.8g,溶解时放热 |
| 加热 | 不分解 | 发生分解反应,分解产物为碳酸钠、二氧化碳和水. |
查看答案和解析>>
科目: 来源: 题型:解答题
| / | OH- | Cl- | SO42- | CO32- |
| H+ | 溶、挥 | 溶 | 溶、挥 | |
| Na+ | 溶 | 溶 | 溶 | 溶 |
| Ba2+ | 溶 | 溶 | 不 | 不 |
| Mg2+ | 不 | 溶 | 溶 | 微 |
查看答案和解析>>
科目: 来源: 题型:解答题
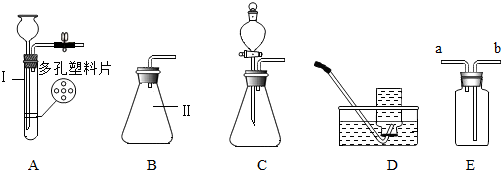
 在实验室利用如图所示装置制取气体,请回答有关问题.
在实验室利用如图所示装置制取气体,请回答有关问题.查看答案和解析>>
科目: 来源: 题型:填空题
 化学反应也有“悄悄”进行的.小明和他的同学对二氧化碳与氢氧化钠溶液的反应进行了如下探究.
化学反应也有“悄悄”进行的.小明和他的同学对二氧化碳与氢氧化钠溶液的反应进行了如下探究.| 实验操作 | 实验现象 | 实验结论 |
| ①取一定量试管中的溶液于试管中,加入足量CaCl2溶液,过滤;②向滤液滴加适量酚酞试液. | 酚酞试液变红 | 小刚猜想成立 |
| 实验操作 | 实验现象 | 实验结论 | |
| 方案一 | 在氢氧化钠溶液中滴加1~2滴酚酞试液,再向其中滴加稀硫酸 | 酚酞试液由红色变为无色 | 氢氧化钠和稀硫酸发生了反应. |
| 方案二 | 在常温的氢氧化钠溶液中滴加同温稀硫酸用温度计测量混合液的温度 | 混合液温度明显升高 |
查看答案和解析>>
科目: 来源: 题型:选择题
| 选项 | 物质 | 操作方法 |
| A | CaO粉末(CaCO3粉末) | 加足量的水,充分搅拌后过滤 |
| B | Fe(Fe2O3) | 加入过量稀盐酸,充分反应后过滤 |
| C | CuSO4溶液(H2SO4) | 加入过量CuO粉末,加热,充分反应后过滤 |
| D | CO2(HCl) | 通过盛有氢氧化钠溶液的洗气瓶 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 补血营养品红桃K中添加微量铁粉,作为补铁剂 | |
| B. | 中秋月饼包装袋内有小袋铁粉,作为干燥剂 | |
| C. | 苏打饼干包装盒中有小袋生石灰,作为补钙剂 | |
| D. | 卤制品中加入大量亚硝酸钠,作为保鲜剂 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 单质:金属单质和非金属单质 | B. | 空气:氮气、氧气和稀有气体等 | ||
| C. | 溶液:饱和溶液和不饱和溶液 | D. | 物质:纯净物和混合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com