
科目: 来源: 题型:解答题
| 实验步骤 | 能观察到的明显现象 | 原因或解释(有化学方程式的就只要写化学方程式) |
| 1.将一小块该鸡蛋壳在酒精喷灯(提供高温)上灼烧 | 有烧焦羽毛的味道 | |
| 2.将灼烧后的鸡蛋壳冷却后研细,投入盛有30mL水的烧杯中,滴入2~3滴酚酞试液 | 溶液变成红色 | |
| 3.继续向烧杯中不断滴加过量的稀盐酸 |
查看答案和解析>>
科目: 来源: 题型:解答题
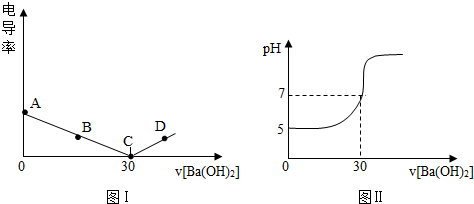
查看答案和解析>>
科目: 来源: 题型:解答题
 我国化工专家侯德榜曾为世界制碱工业做出了突出贡献.“侯氏制碱法”是以食盐、氨气、二氧化碳等为原料先制得碳酸氢钠,进而生产出纯碱.其生产过程用化学方程式可简要表示为:
我国化工专家侯德榜曾为世界制碱工业做出了突出贡献.“侯氏制碱法”是以食盐、氨气、二氧化碳等为原料先制得碳酸氢钠,进而生产出纯碱.其生产过程用化学方程式可简要表示为:查看答案和解析>>
科目: 来源: 题型:解答题
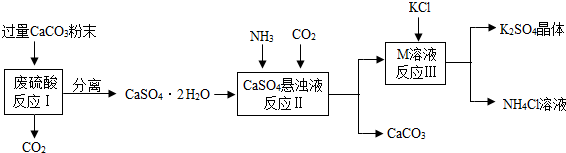
| 物质 | KCl | K2SO4 | NH4Cl | M |
| 溶解度/g(25℃) | 34.0 | 11.1 | 37.2 | 19.5 |
查看答案和解析>>
科目: 来源: 题型:解答题
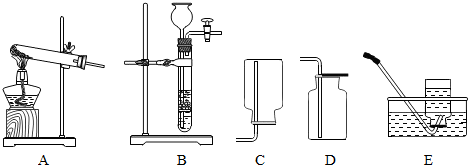
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 将50g氯化钠固体放入50g水中,可配成质量分数为50%的氯化钠溶液 | |
| B. | 50mL水和50mL酒精配制成100mL酒精溶液 | |
| C. | pH值为1和3的两种酸溶液按一定比例混合可得pH值为4的溶液 | |
| D. | 50g溶质质量分数10%的氯化钠加热蒸发25g水,得溶质质量分数等于20%的氯化钠溶液 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 用灼烧法鉴别羊毛和化纤 | B. | 用食盐水制作叶脉书签 | ||
| C. | 用回火后的钢针制作鱼钩 | D. | 用紫甘蓝和酒精溶液制酸碱指示剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com