
科目: 来源: 题型:填空题

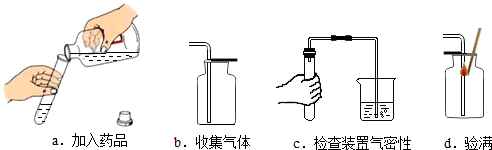
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 硬度比铝大 | B. | 可溶于水 | C. | 具有导电性 | D. | 具有可燃性 |
查看答案和解析>>
科目: 来源: 题型:解答题
| 实验操作 | 实验现象 | 结论 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
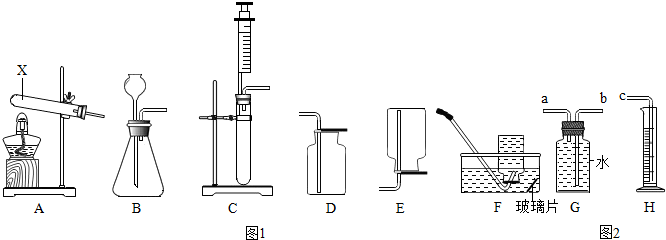
查看答案和解析>>
科目: 来源: 题型:解答题
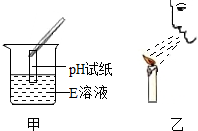 甲、乙两位同学做如下两个实验,请回答:
甲、乙两位同学做如下两个实验,请回答:查看答案和解析>>
科目: 来源: 题型:解答题
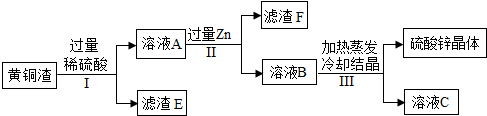
查看答案和解析>>
科目: 来源: 题型:解答题
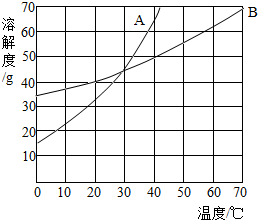 如图是A物质和B物质的溶解度曲线,回答下列问题:
如图是A物质和B物质的溶解度曲线,回答下列问题:查看答案和解析>>
科目: 来源: 题型:解答题
 用如图所示装置,在常温下,分别进行研究燃烧条件和研究氧气性质的实验.已知:白磷的着火点为40℃,实验时打开导管中的开关.
用如图所示装置,在常温下,分别进行研究燃烧条件和研究氧气性质的实验.已知:白磷的着火点为40℃,实验时打开导管中的开关.| 内容 步骤 | 【实验1】研究燃烧条件 | 【实验2】研究氧气性质 |
| Ⅰ | 烧杯中盛有80℃的热水,分别在燃烧匙和 烧杯中导管口放置一 小块白磷,塞紧瓶塞 | 烧杯中盛有NaOH溶液,燃烧匙中放入木炭,点燃木炭后迅速将燃烧匙伸入瓶中,塞紧瓶塞 |
| Ⅱ | 推入适量H2O2 溶液 | 推入适量H2O2 溶液 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com