
科目: 来源: 题型:选择题
| A. | 干冰用于进行人工降雨 | B. | 用白醋除水垢 | ||
| C. | 用竹炭吸附异味 | D. | 用铜丝做导丝 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
 如图为制取氢气的装置图,实验时先打开弹簧夹,再打开分液漏斗活塞a.
如图为制取氢气的装置图,实验时先打开弹簧夹,再打开分液漏斗活塞a.查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:填空题
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 溶解度/g | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | 48.3 | 51.1 |
查看答案和解析>>
科目: 来源: 题型:填空题
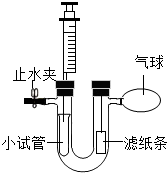 如图所示装置中U形管左侧内固定一支小试管,右侧滤纸条用指示剂浸湿.
如图所示装置中U形管左侧内固定一支小试管,右侧滤纸条用指示剂浸湿.查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题

查看答案和解析>>
科目: 来源: 题型:选择题
| A. | X-S Y-H2SO4 | B. | X-Na2CO3 Y-O2 | C. | X-Fe Y-CaCl2 | D. | X-CO Y-Ca(OH)2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com